 p Imagem dos implantes cirúrgicos, coberto com nanopartículas de ouro (pilha de telas à esquerda) em comparação com as telas cirúrgicas originais anteriores ao tratamento (pilha de telas à direita). Crédito:ICFO
p Imagem dos implantes cirúrgicos, coberto com nanopartículas de ouro (pilha de telas à esquerda) em comparação com as telas cirúrgicas originais anteriores ao tratamento (pilha de telas à direita). Crédito:ICFO
p Inventado há cerca de 50 anos, malhas médicas cirúrgicas tornaram-se elementos-chave nos procedimentos de recuperação de cirurgias de tecidos danificados, o mais frequente sendo o reparo de hérnia. Quando implantado no tecido do paciente, o design flexível e confortável dessas telas ajuda a manter os músculos firmes e permite que os pacientes se recuperem muito mais rápido do que com a cirurgia convencional de semeadura e costura. p Contudo, a inserção de um implante médico no corpo de um paciente traz consigo o risco de contaminação bacteriana durante a cirurgia e a subsequente formação de um biofilme infeccioso sobre a superfície da tela cirúrgica. Esses biofilmes tendem a agir como um revestimento impermeável, impedindo qualquer tipo de agente antibiótico de atingir e atacar as bactérias formadas no filme para interromper a infecção. Assim, terapias com antibióticos, que são limitados no tempo, pode falhar contra essas bactérias superresistentes e o paciente pode acabar em cirurgias recorrentes que podem até levar à morte. De fato, de acordo com a Rede Europeia de Vigilância da Resistência Antimicrobiana (EARS-Net), em 2015, mais de 30, 000 mortes na Europa foram associadas a infecções por bactérias resistentes a antibióticos.
p No passado, várias abordagens têm sido procuradas para prevenir a contaminação do implante durante a cirurgia. Protocolos assépticos pós-cirurgia foram estabelecidos e implementados para combater essas bactérias resistentes a antibióticos, mas nenhum cumpriu inteiramente o papel de resolver esse problema.
p Em um estudo recente publicado em
Nano Letras e destacado em
Nature Photonics , Pesquisadores do ICFO, Dr. Ignacio de Miguel, Arantxa Albornoz, liderado pelo ICREA Prof. no ICFO Romain Quidant, em colaboração com os pesquisadores Irene Prieto, Dra. Vanesa Sanz, Dra. Christine Weis e Dr. Pau Turon da principal empresa de dispositivos médicos e farmacêuticos B. Braun, desenvolveram uma nova técnica que usa nanotecnologia e fotônica para melhorar drasticamente o desempenho das telas médicas para implantes cirúrgicos.
p Por meio de uma colaboração contínua desde 2012, a equipe de pesquisadores do ICFO e B. Braun Surgical, S.A., desenvolveu uma malha médica com uma característica particular:a superfície da malha foi quimicamente modificada para ancorar milhões de nanopartículas de ouro. Porque? Porque as nanopartículas de ouro comprovadamente convertem luz em calor de maneira muito eficiente em regiões muito localizadas.
 p Micrografias SEM do S. aureus biofilme formado na superfície da tela cirúrgica. Crédito:ICFO
p Micrografias SEM do S. aureus biofilme formado na superfície da tela cirúrgica. Crédito:ICFO
p A técnica de usar nanopartículas de ouro em processos de conversão luz-calor já havia sido testada em tratamentos de câncer em estudos anteriores. Ainda mais, no ICFO esta técnica foi implementada em vários estudos anteriores apoiados pela Fundação Cellex, sendo, portanto, outro exemplo saliente de como o apoio filantrópico visionário precoce, dirigido ao enfrentamento de problemas fundamentais, acaba levando a importantes aplicações práticas. Para este caso particular, em saber que mais de 20 milhões de operações de reparo de hérnia acontecem todos os anos em todo o mundo, eles acreditavam que este método poderia reduzir os custos médicos em operações recorrentes, eliminando os tratamentos com antibióticos caros e ineficazes que estão sendo empregados atualmente para resolver este problema.
p Assim, em seu experimento in vitro e por meio de um processo completo, a equipe revestiu a malha cirúrgica com milhões de nanopartículas de ouro, espalhando-os uniformemente por toda a estrutura. Eles testaram as malhas para garantir a estabilidade a longo prazo das partículas, a não degradação do material, e o não desprendimento ou liberação de nanopartículas para o ambiente circundante (frasco). Eles foram capazes de observar uma distribuição homogênea das nanopartículas sobre a estrutura usando um microscópio eletrônico de varredura.
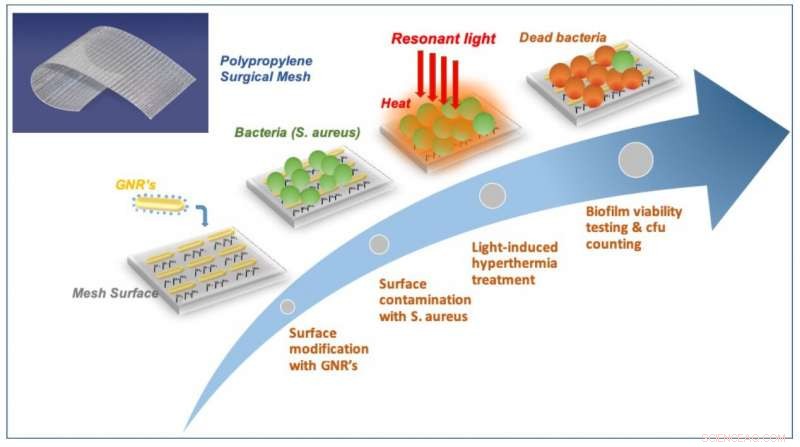 p Visão esquemática da prevenção de biofilme habilitado para plasmon em telas cirúrgicas. Crédito:ICFO
p Visão esquemática da prevenção de biofilme habilitado para plasmon em telas cirúrgicas. Crédito:ICFO
p Assim que a malha modificada estiver pronta, a equipe o expôs à bactéria S.aureus por 24 horas até observar a formação de um biofilme na superfície. Subseqüentemente, eles começaram a expor a malha a pulsos curtos e intensos de luz infravermelha próxima (800 nm) durante 30 segundos para garantir que o equilíbrio térmico fosse alcançado, antes de repetir este tratamento 20 vezes com 4 segundos de intervalos de descanso entre cada pulso. Eles descobriram o seguinte:em primeiro lugar, eles viram que iluminar a malha na frequência específica induziria ressonâncias plasmônicas de superfície localizadas nas nanopartículas - um modo que resulta na conversão eficiente de luz em calor, queimar as bactérias na superfície. Em segundo lugar, usando um microscópio confocal de fluorescência, eles viram o quanto da bactéria havia morrido ou ainda estava viva. Para as bactérias que permaneceram vivas, eles observaram que as bactérias do biofilme se tornaram células planctônicas, recuperar sua sensibilidade ou fraqueza em relação à terapia com antibióticos e à resposta do sistema imunológico. Para as bactérias mortas, eles observaram que ao aumentar a quantidade de luz fornecida à superfície da malha, a bactéria perderia sua aderência e se desprenderia da superfície. Em terceiro lugar, eles confirmaram que operar em faixas de luz infravermelha próximas era completamente compatível com as configurações in vivo, o que significa que essa técnica provavelmente não danificaria o tecido saudável circundante. Finalmente, eles repetiram o tratamento e confirmaram que o aquecimento recorrente da malha não havia afetado suas capacidades de eficiência de conversão.
p Como ICREA Prof no ICFO Romain Quidant comenta, "os resultados deste estudo abriram caminho para o uso de nanotecnologias de plasmon para prevenir a formação de biofilme bacteriano na superfície dos implantes cirúrgicos. Ainda existem várias questões que precisam ser abordadas, mas é importante enfatizar que tal técnica realmente significam uma mudança radical nos procedimentos de operação e posterior recuperação do paciente após a recuperação. "
p Dr. Pau Turon, Diretor de Pesquisa e Desenvolvimento da B. Braun Surgical, S.A. explica, "nosso compromisso em ajudar os profissionais de saúde a evitar infecções hospitalares nos leva a desenvolver novas estratégias para combater bactérias e biofilmes. a equipe de pesquisa está explorando a possibilidade de estender essa tecnologia a outros setores onde os biofilmes devem ser evitados. "


