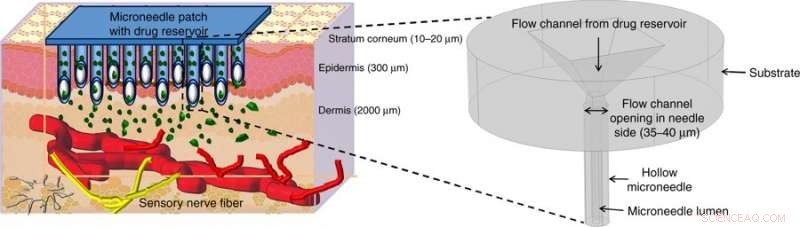
Distribuição de droga ilustrada usando microagulhas ocas (MNs). Os MNs ocos perfuram a pele para alcançar acima dos nervos sensores da dor na região transdérmica da pele e liberam o medicamento sem dor por meio de métodos de ativação adequados. A figura do início mostra uma visão ampliada da estrutura da microagulha proposta neste trabalho. Crédito:Microsystems &Nanoengineering, doi:https://doi.org/10.1038/s41378-018-0039-9.
As microagulhas são projetadas para infundir medicamentos por via transdérmica (através da pele) e relativamente sem dor durante as aplicações clínicas. Em um estudo recente, Richa Mishra e seus colegas desenvolveram uma nova técnica para converter filmes de polímero em uma forma vítrea de carbono resistente a fraturas para desenvolver microagulhas. O dispositivo de entrega transdérmica otimizado de drogas foi fabricado usando fotolitografia para formar uma microagulha biocompatível e robusta para aplicações pré-clínicas.
Os cientistas primeiro geraram uma série de verticais, tubos ocos feitos de polímero à base de epóxi SU-8 em um substrato de silício. As microestruturas foram afiadas em formas semelhantes a agulhas por tratamento térmico em um forno livre de oxigênio e o produto final foi composto inteiramente de átomos de carbono ordenados aleatoriamente. A caracterização subsequente dos materiais incluiu nanoindentação para medir a rigidez da superfície. As estruturas de carbono vítreo eram robustas o suficiente para penetrar na pele humana sem quebrar. Os resultados do estudo foram publicados em Microsistemas e Nanoengenharia .
Os autores detalharam o processo do sistema convencional de carbono-microeletromecânico (C-MEMS) usado para fabricar as microagulhas. No processo, Mishra et al. usou uma etapa escalável e irreversível de pirólise, onde o precursor de microagulhas SU-8 pré-padronizadas foram convertidas em estruturas de carbono vítreo. Os experimentos foram conduzidos em uma atmosfera inerte a altas temperaturas (~ 900 0 C) para reter sua forma original após o encolhimento. Na conversão para carbono vítreo, as microagulhas herdaram as propriedades associadas de dureza, biocompatibilidade, resistência térmica e química.
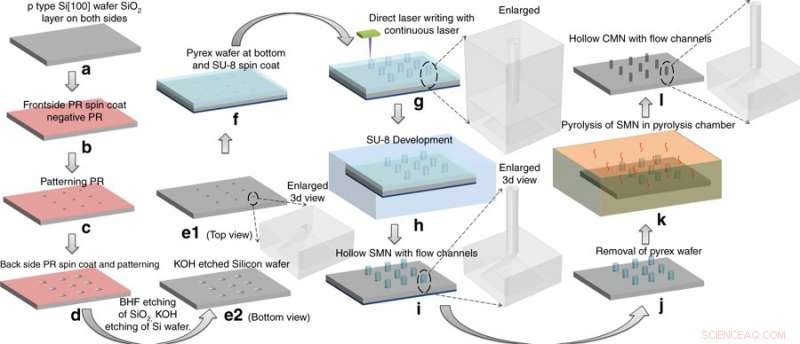
Processo de fabricação:conversão de microagulhas SU-8 (SMNs) em microagulhas de carbono vítreo oco (CMNs) por pirólise. As estruturas SMN encolheram, mantendo sua geometria geral. Crédito:Microsystems &Nanoengineering, doi:https://doi.org/10.1038/s41378-018-0039-9
Os pesquisadores compararam a dureza e o módulo de Young do carbono e das microagulhas SU-8 para entender o aumento da resistência induzida pelo processo C-MEMS. O encolhimento estrutural das microagulhas de carbono na pirólise foi estimado a partir daí. Mishra et al. conduziu caracterização de materiais em profundidade com espectroscopia de raios-X de dispersão de energia (EDX) para entender a química de superfície e espectroscopia Raman para estimar a porcentagem atômica de carbono na estrutura cristalina da microagulha.
Os resultados confirmaram a composição vítrea das microagulhas. Testes adicionais de compressão e flexão determinaram as forças máximas que as microagulhas podiam suportar. Os dispositivos podiam suportar forças que eram aproximadamente duas ordens de magnitude maiores do que as forças resistivas da pele. Os dispositivos foram posteriormente testados na superfície da pele de um modelo de mouse no estudo.
O uso de carbono na medicina não é novo; exemplos incluem aplicações em articulações ortopédicas, como fibras / compostos de carbono em cirurgias ortopédicas e como materiais em instrumentos cirúrgicos. As propriedades das fibras de carbono em formar estruturas semelhantes a andaimes 3-D têm demonstrado capacidade promissora na regeneração do tecido ósseo. As propriedades personalizadas do carbono os tornaram adequados para fabricar microagulhas de administração transdérmica (MN) para administração avançada de drogas e vacinas.
Por competência, Os MNs devem ter um comprimento ideal para a entrega eficaz do medicamento, mas seja curto o suficiente para evitar causar dor. Cientistas de materiais estão explorando estratégias para selecionar materiais e métodos clinicamente viáveis que podem ser traduzidos comercialmente em um curto período de tempo.
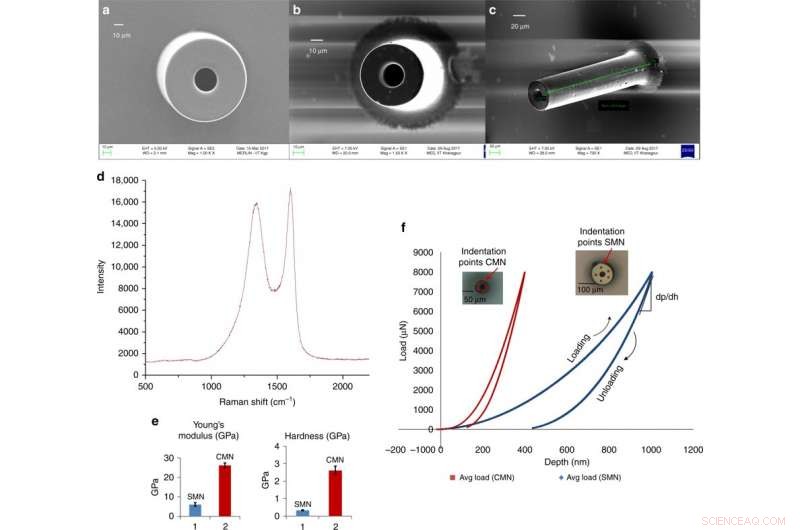
Microagulhas de carbono vítreo para distribuição transdérmica de drogas derivadas de um processo C-MEMS escalável. a) Micrografia eletrônica de varredura de um SMN (diâmetro externo de 100 μm, diâmetro interno 50 μm). b) MN pirolisado correspondente. c) Vista inclinada do mesmo CMN. d) Espectro Raman da microagulha de carbono. e) Comparação do módulo de Young e dureza para o SU-8 e MNs de carbono. f) Dados de carga vs. deslocamento para um SMN e o correspondente CMN pirolisado. Crédito:Microsystems &Nanoengineering, doi:https://doi.org/10.1038/s41378-018-0039-9.
Os principais requisitos para MNs incluem biocompatibilidade, força e liberação controlada de drogas. MNs sólidos podem ser desenvolvidos com polímeros, silício, aço, titânio e níquel por meio de processos subtrativos ou aditivos. Uma desvantagem dos MNs sólidos é sua capacidade limitada de distribuição ideal de drogas. Por outro lado, MNs ocos podem ser anexados a um reservatório de droga com pressão externa para distribuição ideal de droga.
Mishra et al. escolheu o precursor SU-8 por sua alta força de reticulação, biocompatibilidade, baixo custo, polimerização induzida por luz e compatibilidade com o processo da indústria microeletrônica. Para fabricar oco, microagulhas de carbono vítreo (CMNs), o processo C-MEMS foi primeiro adaptado para padronizar microagulhas SU-8 (SMNs) usando gravação direta a laser, seguido por sua conversão em CMNs vítreos via pirólise. Portas microfluídicas foram gravadas em um wafer de silício, de acordo com um protocolo anterior desenvolvido pela mesma equipe de pesquisa. Os produtos resultantes (CMNs) foram caracterizados por suas propriedades mecânicas, incluindo dureza e módulo de Young em comparação com seus precursores SMNs. Os resultados indicaram que os CMNs foram superiores.
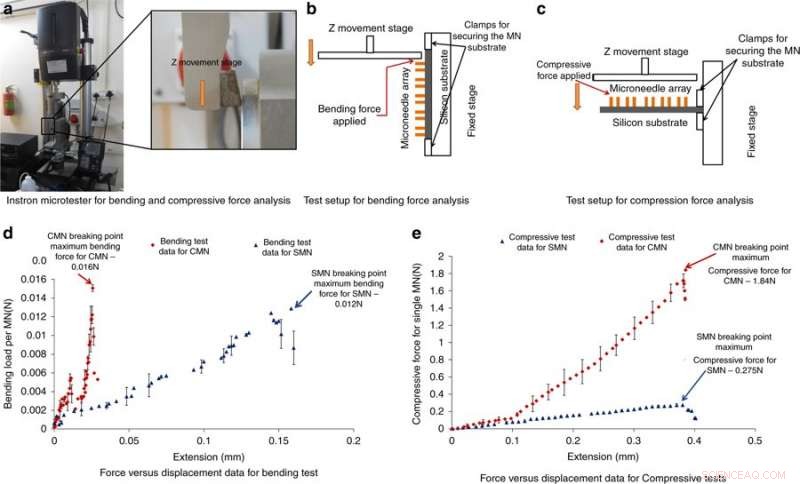
Microtester Instron para análise e resultados da força de flexão e compressão. a) Fotografia do microtester Instron empregado para análise da força de flexão e compressão. b) Configuração de teste para análise da força de flexão. c) Configuração de teste para análise da força de compressão. d) Resultados de força vs. deslocamento do teste de flexão. e) Resultados de força vs. deslocamento do teste de compressão. Crédito:Microsystems &Nanoengineering, doi:https://doi.org/10.1038/s41378-018-0039-9
Mishra et al. observaram e quantificaram as dimensões dos precursores SMN e as estruturas CMN pirolisadas correspondentes usando imagens de microscopia eletrônica de varredura (MEV). Após a pirólise, o diâmetro e a espessura da parede da microagulha diminuíram. Os resultados de EDX mostraram aumento da porcentagem atômica de elementos de carbono para MNs de carbono. A ausência de nitrogênio na composição da microagulha de carbono indicou sua remoção durante o aquecimento. O percentual de conteúdo de oxigênio foi devido à estrutura CMN e ao Si / SiO 2 superfície do substrato. A espectroscopia Raman mostrou a natureza cristalina vítrea da microestrutura final por meio da verificação do produto de carbono. Os resultados estão de acordo com estudos anteriores.
Os cientistas obtiveram dados de deslocamento de carga por meio de nanoindentação para as estruturas separadas de SU-8 e de carbono. Eles calcularam a dureza e o módulo de elasticidade usando o modelo Oliver Pharr. Os resultados mostraram uma dureza de 0,33 GPa e módulo de Young de 5,52 GPa para SMN. Na conversão para CMN via pirólise, os resultados de indentação mostraram maior elasticidade do material, a dureza aumentou oito vezes para 2,62 GPa e o módulo de Young aumentou 4,8 vezes para 26,97 GPa.
Para entender a capacidade dos MNs de suportar forças sem quebra durante a inserção na pele, Mishra et al. realizaram medições da força de flexão e compressão da estrutura. Tipicamente, um MN experimenta resistência durante a penetração na pele, a força aplicada deve, portanto, ser maior do que a força oposta. Para testar dobra / compressão, os MNs foram carregados em um microtestador Instron e uma placa de metal foi direcionada para os MNs até que se quebrassem; se a carga aplicada estava abaixo da força máxima de compressão ou flexão, as agulhas não vão quebrar. Uma queda brusca na força de compressão ou força de flexão indicou um ponto de fratura. Os resultados mostraram que os CMNs eram muito mais fortes do que os precursores, permitindo-lhes superar a resistência durante a penetração na pele.
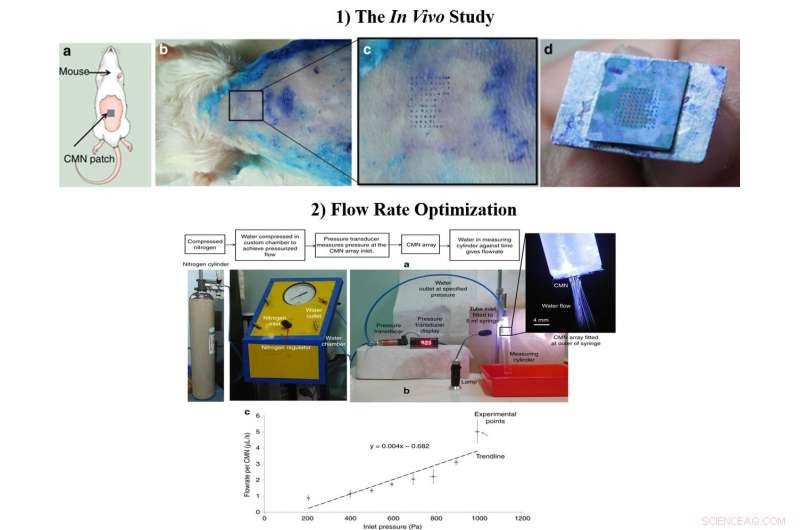
1) O estudo in vivo a) Esquema do teste de inserção de MN em camundongos. b) Teste de inserção biológica realizado em camundongos Swiss Albino de 6 a 8 semanas de idade. c) Visão ampliada da área da pele perfurada pelos CMNs. d) Matriz intacta de 10 × 10 após múltiplas inserções. 2) A taxa de fluxo otimizada, a) Configuração de teste para medição de taxa de fluxo. b) Taxa de fluxo por microagulha em diferentes pressões de entrada. Crédito:Microsystems &Nanoengineering, doi:https://doi.org/10.1038/s41378-018-0039-9
Depois de confirmar o caráter mecânico e a superioridade dos CMNs ocos no laboratório, Richa Mishra e colegas de trabalho conduziram experimentos in vivo para testar os CMNs na pele de camundongos. Uma matriz de microagulhas recentemente mergulhada em azul de metileno foi pressionada sobre a pele de um modelo de camundongo albino suíço e lentamente retirada várias vezes. As marcas da agulha de azul de metileno eram visíveis, os MNs permaneceram intactos após múltiplas inserções e um espaçamento de matriz de 500 µm foi ideal para estudos posteriores em laboratório.
Os cientistas otimizaram as dimensões do fluxo durante o processo de fabricação e incluíram conduítes microfluídicos com tamanho reduzido para funcionalidade MN aprimorada. Para testar as taxas de fluxo, eles anexaram uma seringa de 5 mL com uma câmara personalizada contendo água deionizada. Quando os cientistas mediram a taxa de fluxo média versus pressão para MNs individuais, os resultados mostraram que a distribuição da droga poderia ser controlada, em última instância, modificando a pressão de entrada.
A técnica definitiva de caracterização de materiais no estudo foi a nanoindentação, já o parâmetro quantificou a dureza superficial e o módulo de Young para verificar a superioridade dos CMNs. O trabalho futuro incluirá o desenvolvimento de entrega controlada de drogas, com uma microbomba e um reservatório de medicamento integrado ao projeto MN. Desta maneira, os cientistas pretendem desenvolver sistemas avançados de entrega de medicamentos e vacinas na área da saúde que sejam econômicos, preciso e indolor para o paciente.
© 2019 Science X Network