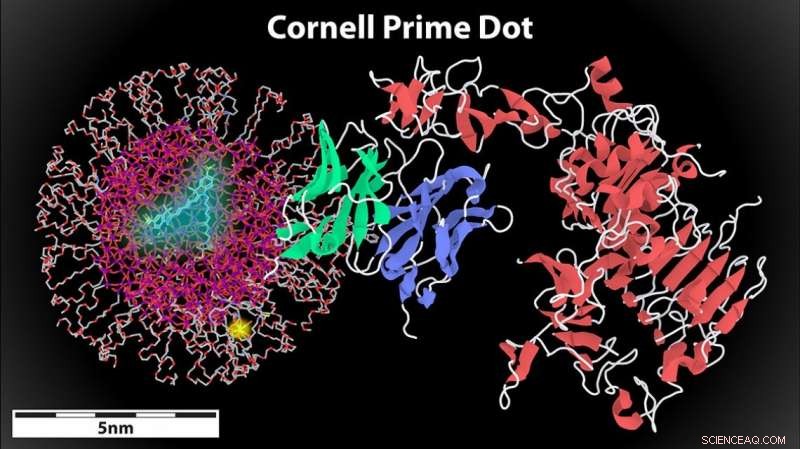
Uma renderização do ponto principal de Cornell (à esquerda) com um fragmento de anticorpo anexado (centro) ligando-se a um receptor de células cancerígenas HER2 (à direita). O ponto e o anexo de anticorpo combinados têm menos de 8 nanômetros de diâmetro, o limite para a depuração renal. Crédito:Cornell University
A imagem baseada em anticorpos de uma forma particularmente agressiva de câncer de mama está passando por testes clínicos em todo o mundo, mas o caminho do teste à aplicação está sendo dificultado por um grande obstáculo:a segurança.
As preocupações decorrem da segmentação ineficiente de tumor, que pode resultar em acúmulo na medula óssea, fígado e rins do material radioativo necessário para a imagem. Esforços recentes têm se concentrado em veículos de entrega em nanoescala com componentes imunológicos, mas esses veículos muitas vezes ainda são muito grandes (20 nanômetros ou mais) para a depuração renal após a obtenção de imagens.
Ulrich Wiesner, o Spencer T. Olin Professor de Engenharia em ciência de materiais e engenharia na Cornell University, em colaboração com a Dra. Michelle Bradbury do Memorial Sloan Kettering Cancer Center (MSKCC) e Weill Cornell Medicine, propôs uma nova abordagem usando nanopartículas de sílica ultra-pequenas - mais conhecidas como "pontos Cornell" (ou pontos C) - inventadas em seu laboratório há mais de 12 anos.
Sua equipe - incluindo pesquisadores da empresa farmacêutica MedImmune - equipou os pontos C com fragmentos de anticorpos. Como os conjugados resultantes são menores que 8 nanômetros, esses pontos C permitem a depuração renal ao mesmo tempo em que atingem a especificidade necessária para o direcionamento eficiente do tumor.
Eles relatam sua descoberta em "Nanopartículas direcionadas ultra-pequenas com fragmentos de anticorpos projetados para detecção por imagem de câncer de mama superexpressando HER2, "publicado em 8 de outubro em Nature Communications . Feng Chen, cientista pesquisador sênior no MSKCC, e Kai Ma, pesquisador de pós-doutorado no laboratório Wiesner, são co-autores principais.
Wiesner disse que esta pesquisa cria "uma nova pista" para empregar fragmentos de anticorpos para uma série de doenças, câncer em particular, e para diagnósticos, bem como distribuição de medicamentos - quando combinados em uma única entidade, também conhecida como "teranóstica".
"Esta é a primeira vez que trabalhamos com esses fragmentos de anticorpos, "Wiesner disse, "aproveitando assim o poder dos anticorpos na luta contra o câncer."
Cornell dots e sua geração mais recente - denominados "Cornell prime dots, "ou simplesmente C 'dots - evoluíram desde que Wiesner e seu grupo os introduziram em 2005 e, desde então, em colaboração com Bradbury, um primeiro ensaio clínico os considerou seguros para humanos em 2014. Dois anos atrás, os pontos mostraram ter a capacidade não apenas de detectar células cancerosas, mas de serem autoterapêuticos, matando-as de fato.
Esta última pesquisa coloca os pontos C de volta no papel de localizador de câncer, mas adiciona um "localizador de tumor" na forma de um fragmento de anticorpo. Eles usaram um fragmento específico do anticorpo em forma de Y, em oposição à molécula inteira, para manter o ponto C 'dentro do limite de tamanho para a depuração renal.
O alvo:câncer de mama HER2-positivo, mais agressivo e mortal do que o câncer HER2-negativo, tornando-o um alvo atraente para novos diagnósticos e terapias. Na colaboração, A MedImmune projetou um fragmento de anticorpo especificamente para direcionar a proteína HER2 e um local de conjugação que não interfere com sua atividade de ligação. Os grupos de Wiesner e Bradbury, Enquanto isso, trabalharam juntos para anexá-lo à superfície do ponto C 'para manter o conjugado geral abaixo de 8 nanômetros de diâmetro.
O ponto em si foi sintetizado de uma forma que deu a ele cinco funções distintas, tudo dentro de seu tamanho ultrapequeno de 6 a 7 nanômetros.
O direcionamento in vitro e in vivo (camundongo) de células de câncer de mama HER2-positivas foi bem-sucedido, com absorção tumoral in vivo dos pontos injetados de até 17,2 por cento, o mais alto que Wiesner e Bradbury alcançaram em todas as suas pesquisas de pontos C.
"A injeção circula pelo sangue e precisa escapar da vasculatura, tem que se difundir através do tecido conjuntivo, tem que se associar ao tumor e então meio que penetrar no corpo do tumor, "Wiesner disse." Queremos 100 por cento - todo mundo quer 100 por cento. Mas quando você considera todas as outras coisas que estão competindo pelo veículo em outras partes do corpo, 17 por cento não é tão pequeno. "
Bradbury, que, junto com Wiesner, dirige o MSK-Cornell Center for Translation of Cancer Nanomedicines, chama o ponto C 'de um "divisor de águas" na distribuição de medicamentos à base de nanopartículas.
"Essas descobertas da pesquisa são muito empolgantes, " ela disse, "como eles sugerem que poderíamos entregar especificamente uma variedade de terapias de pequenas moléculas - quimioterapia, inibidores e radioterapia - sem a toxicidade normalmente encontrada com sondas de partículas maiores. "