Nanopartículas de ferro amorfo apresentam toxicidade específica em células tumorais. No jornal Angewandte Chemie , Cientistas chineses descrevem seu projeto e síntese de um estado amorfo especial de ferro nanoparticulado, que pode liberar localmente espécies reativas de ferro no ambiente ácido e rico em peróxido de hidrogênio das células cancerosas, proporcionando novas possibilidades para terapias teranósticas e quimodinâmicas.
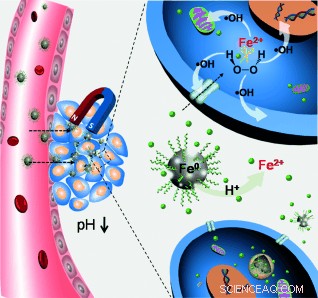
As células cancerosas são caracterizadas por seu ambiente celular relativamente ácido e pela produção de quantidades significativas de peróxido de hidrogênio em comparação com as células saudáveis. Algumas abordagens quimodinâmicas para o tratamento do câncer, portanto, empregam a reação de Fenton, isso é, íons de ferro reagindo com o peróxido de hidrogênio para produzir espécies reativas de oxigênio (ROS), o que, por sua vez, pode danificar e destruir as células cancerosas. Contudo, o transporte de íons de ferro para as células-alvo é problemático, e as nanopartículas de ferro cristalino não são tão eficazes. Portanto, Jianlin Shi e Wenbo Bu e seus grupos no Instituto de Cerâmica de Xangai, em colaboração com a Universidade Fudan de Xangai, China, já prepararam nanopartículas de ferro em uma forma amorfa, estado vítreo. "Interessantemente, as nanopartículas de ferro amorfo (0) apresentam várias propriedades físico-químicas únicas, "os cientistas escrevem, e:"Os resultados confirmam que as nanopartículas de ferro amorfo, peróxido de hidrogênio, e as condições ácidas agem sinergicamente para matar as células. "
Além de seu potencial como drogas, outras vantagens são um bom contraste para imagens de ressonância magnética e a possibilidade de direcionamento magnético. "Idealmente, um transportador perfeito deve liberar sua carga de uma vez quando ela é transferida de condições neutras para levemente ácidas, como aqueles no microambiente tumoral, "escrevem os autores. Usando imagens de ressonância magnética, eles provaram por testes in vitro e in vivo que o mecanismo previsto estava funcionando.
Segmentação magnética, por outro lado, permite a entrega do medicamento ao tecido alvo por meio de magnetização. Os cientistas observaram que "a retenção magnética eficiente foi alcançada in vivo, fornecendo uma boa base para a terapia quimiodinâmica. "No entanto, eles também dizem que as perspectivas futuras incluirão a modificação da superfície das partículas para melhorar ainda mais o desempenho de segmentação do tumor. Em poucas palavras, A elegante abordagem de "bolha do hubble" de Shi e Bu, como eles chamam, produziu um minúsculo, cavalo de Tróia altamente eficaz para terapia quimio-dinâmica do câncer, como mostrado em ratos. O método de preparação apresenta condições amenas e também perspectivas para outros metais.