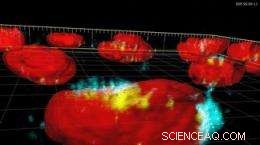
Foto:Partículas superparamagnéticas de óxido de ferro (azul e amarelo) absorvidas no núcleo de uma célula (núcleo em vermelho).
(PhysOrg.com) - Detectando células cancerosas e destruindo-as, injetar drogas com extrema precisão em células doentes no corpo humano - estes são apenas dois exemplos do que os cientistas da EPFL estão tentando realizar usando nanopartículas de óxido de ferro desenvolvidas no Laboratório de Tecnologia de Pó da Escola (LTP).
Apenas 5 a 10 nanômetros de diâmetro (um nanômetro é um milionésimo de um milímetro), as nanopartículas de óxido de ferro superparamagnéticas que estão sendo estudadas pela equipe de LTP do professor Heinrich Hofmann são promissoras, porque eles exibem propriedades magnéticas quando expostos a um campo magnético externo. Essa característica é importante para certas aplicações médicas, como o diagnóstico de doenças como artrite, localizar tumores, e destruindo células cancerosas em pacientes.
Detectando câncer
Os cientistas da EPFL estão analisando três aplicações principais:diagnósticos, tratamento e eliminação de células malignas. “Na prática, partículas de óxido de ferro já são usadas como agentes de contraste em imagens de ressonância magnética (MRI) em casos de tumor de fígado, ”Observa Hofmann. “Estamos estudando como aplicar esse método a todos os tipos de tumores e, se possível, a outras doenças, como artrite. Este último é o objetivo de um grande projeto EU FP-7 (Nanodiara). ”É assim que funciona:as células cancerosas têm receptores em sua superfície, uma espécie de ID de celular. A cobertura das nanopartículas é adaptada em conformidade (por meio de anticorpos, por exemplo), de modo que, uma vez que eles são injetados por via intravenosa, eles só se ligam aos receptores nas células cancerosas. E porque uma partícula de óxido de ferro altera o contraste do tecido quando submetida a um campo magnético, assim, é possível identificar a localização exata das células cancerosas usando a ressonância magnética. “Até agora, esta técnica só foi validada para tumores de fígado, porque para cada tipo de câncer, elementos de superfície devem ser adicionados, que mudam o comportamento das partículas. No entanto, é muito difícil entender o comportamento das nanopartículas em um fluido complexo, como sangue, ”Ele explica.
Tratamento direcionado
Um aspecto da pesquisa se concentra em uma nova aplicação empolgante:a entrega de drogas direcionadas a células específicas. “É possível que as nanopartículas de óxido de ferro penetrem diretamente nas organelas de uma célula. Esta propriedade abre a possibilidade de entregar um medicamento diretamente no interior de uma célula, ”Explica Hofmann. Isso tem vantagens claras sobre os métodos de administração de medicamentos existentes. O professor de radiologia da Universidade de Genebra, Jean-Paul Vallée, diz:
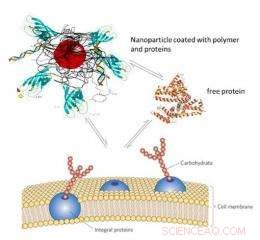
“Nos atuais tratamentos sistêmicos com drogas, a droga não é administrada seletivamente no corpo, mas amplamente absorvido. Com este novo método, seríamos capazes de evitar certos efeitos colaterais e entregar o medicamento apenas às células que precisam ser tratadas. ”
Destruindo tumores com calor
Além de detectar células específicas e entregar drogas diretamente nelas, as partículas de óxido de ferro também têm a capacidade de destruir tumores ósseos hipertermicamente. No câncer ósseo, as metástases freqüentemente se desenvolvem na coluna vertebral. Um tratamento atual envolve a injeção de uma substância semelhante ao cimento nos corpos das vértebras. Uma vez que esta substância à base de polímero está no corpo, ele se solidifica e, assim, estabiliza as vértebras. De acordo com os pesquisadores, se partículas superparamagnéticas foram adicionadas ao cimento antes da injeção, seria possível transferir energia aplicando um campo magnético alternativo externo, aquecendo assim o implante até 46 ° C. Este procedimento destruiria seletivamente as células cancerosas nas proximidades, porque são menos tolerantes ao calor do que os tecidos normais. “Este método seria menos agressivo do que os lasers, que também queimam células saudáveis e deixam resíduos para trás, ”Acrescenta Hofmann.
Para o momento, essas três aplicações estão em estágio pré-clínico, e fazem parte de vários projetos envolvendo vários parceiros, como os Hospitais da Universidade de Lausanne (CHUV), a Universidade de Genebra e o Centro Suíço de Eletrônica e Microtecnologia (CSEM), bem como empresas como ANTIA ou MERCK-Serono.