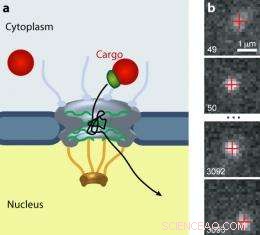
 p O complexo de poros nucleares (NPC) bloqueia o tráfego de todas as moléculas entre o citoplasma e o núcleo das células eucarióticas. (a) Cargas maiores (vermelho) requerem um receptor de transporte (verde) para passar pelo portão. (b) Uma carga de pontos quânticos se move através de um NPC. Imagem:Alan Lowe
p O complexo de poros nucleares (NPC) bloqueia o tráfego de todas as moléculas entre o citoplasma e o núcleo das células eucarióticas. (a) Cargas maiores (vermelho) requerem um receptor de transporte (verde) para passar pelo portão. (b) Uma carga de pontos quânticos se move através de um NPC. Imagem:Alan Lowe
p (PhysOrg.com) - Pesquisadores da UC Berkeley Karsten Weis, Jan Liphardt, e colegas usaram sondas fluorescentes chamadas de pontos quânticos para determinar quais moléculas entram no núcleo por meio de seus nano poros e quais são expelidas de volta. Suas descobertas podem ajudar a desenvolver drogas que podem passar pelos poros e atingir o DNA de uma célula. p Os biofísicos do QB3 traçaram com resolução sem precedentes os caminhos das cargas que se movem através do complexo de poros nucleares (NPC), uma abertura em nanoescala seletiva que controla o acesso ao núcleo da célula, e respondeu a várias perguntas importantes sobre sua função.
p O NPC, um grande conjunto de proteínas em forma de rede de basquete com tentáculos, é a porta de entrada para o núcleo da célula, onde a informação genética é armazenada. Cada núcleo da célula contém cerca de 2, 000 NPCs, embutido no envelope nuclear. O NPC (que tem cerca de 50 nanômetros de largura) é responsável por todo o transporte para dentro e para fora do núcleo. Para evitar que o conteúdo do resto do interior da célula se misture com o do núcleo, o NPC discrimina as cargas com grande precisão.
p Vários vírus têm como alvo o NPC para entrar no núcleo, e o transporte disfuncional entre o citoplasma e o núcleo tem sido implicado em várias doenças, incluindo câncer.
p Os cientistas construíram modelos para o NPC, mas como esse canal opera e atinge sua seletividade permanece um mistério. Sabe-se que, para passar pelo NPC, moléculas grandes devem se ligar a pelo menos alguns receptores chamados “importinas”; se a ligação de mais importinas acelera ou retarda a passagem de uma molécula não está claro. Então, também, tem o ponto exato em que uma proteína transportadora chamada "Ran" desempenha um papel crucial, substituindo uma molécula de GTP (um combustível celular, um análogo do mais conhecido ATP) para um do GDP que a molécula grande traz consigo quando entra no NPC.
p Karsten Weis, um professor de biologia molecular e celular da UC Berkeley, Jan Liphardt, um professor de física da UC Berkeley, e seus colegas conduziram experimentos de imagem avançados que resolveram esses problemas. (Weis e Liphardt são membros do QB3.) A pesquisa foi publicada em 1º de setembro na revista
Natureza , em um artigo no qual o pós-doutorando de Berkeley Alan Lowe e o estudante de graduação Jake Siegel foram os primeiros autores.
p Anteriormente, os cientistas observaram o movimento de pequenas moléculas (alguns nm de diâmetro), rotulados com etiquetas fluorescentes, através do NPC. Mas o trânsito rápido e o sinal fraco dessas moléculas resultaram em esparsos, dados difusos. Lowe, Siegel, et al. empregou "pontos quânticos", que têm cerca de 20 nm de diâmetro - e, portanto, mais lentos do que moléculas menores - e muito mais brilhantes do que os fluoróforos convencionais. Os pesquisadores revestiram os pontos quânticos com sinais reconhecidos por importinas. Usando uma técnica microscópica que lhes permitiu ver um plano, fatia visual fina através de células vivas, eles assistiram centenas de pontos individuais entrando, balançando ao redor, sendo ejetado de, e em alguns casos admitidos por meio de, NPCs. Os pesquisadores gravaram dados de vídeo e acompanharam o movimento de 849 pontos quânticos com precisão nanométrica.
p Os caminhos tipo espaguete dos pontos quânticos, sobrepostos uns aos outros, revelou que as partículas se enquadravam em três classes:“abortos precoces, ”Que foram brevemente confinados e depois rebatidos; “Abortos tardios, ”Que vagou e serpenteava para a extremidade interna do poro antes de sair por onde vieram; e “sucessos, ”Que seguiram os mesmos caminhos dos abortos tardios, mas tiveram permissão para entrar.
p Dos meandros erráticos dos caminhos, os pesquisadores deduziram que os pontos quânticos estavam de fato se difundindo aleatoriamente, em vez de ser transportado ativamente. E adicionar mais importinas ao revestimento dos pontos encurtou o tempo de trânsito, sugerindo que os importins tornam a carga que chega mais solúvel dentro do NPC em vez de se prender às paredes internas.
p Os pesquisadores descobriram um resultado particularmente interessante quando retiraram a proteína transportadora Ran do experimento. Sem Ran na mistura, os pontos quânticos seguiram exatamente o mesmo intervalo de caminhos de quando Ran estava presente, exceto que praticamente nenhum passou pelo NPC.
p Considerando seus dados de caminho, os autores desenharam um modelo de como o NPC opera. Carga grande é inicialmente capturada pela franja de filamento do NPC. Em seguida, encontra uma constrição, através da qual pode entrar numa espécie de antecâmara. Então, em certos casos, Ran troca o PIB da carga por um GTP e é admitido no núcleo. Apenas a etapa final é irreversível.
p "É um estudo elegante, "diz Michael Rout, um professor de biologia celular e estrutural na The Rockefeller University, cuja especialidade é o transporte de NPC. "Se finalmente entendermos como o NPC opera no nível mais sutil, poderíamos talvez construir filtros para selecionar moléculas de interesse. "
p De fato, um dos novos insights principais é que a seletividade do NPC parece resultar de uma cascata de filtros, cada um preferindo cargas corretas, em vez de apenas uma etapa muito seletiva. Isso ajuda a explicar por que algumas coisas podem facilmente entrar no núcleo e outras coisas são excluídas. Esta descoberta pode ter algumas implicações clínicas muito práticas, Liphardt e Weis dizem. Pode permitir que os cientistas desenvolvam técnicas para entregar com eficiência grandes cargas feitas pelo homem, tais como conjugados de droga-polímero e agentes de contraste, para o núcleo, que contém o genoma.
