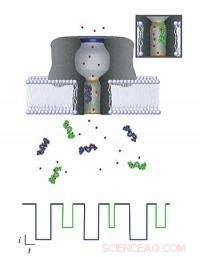
Cada molécula que passa pelo nanopore pode ser identificada monitorando a mudança que ela causa em uma corrente iônica que flui através da membrana. Quando diferentes moléculas (objetos roxos e verdes) entram no poro (verde mostrado na inserção), cada um reduz a corrente por uma certa quantidade e período de tempo (mostrado pelo esquema de cores correspondente no diagrama atual abaixo), dependendo de seu tamanho e capacidade de atrair íons próximos (pontos vermelhos). O modelo NIST pode ser usado para extrair essas informações, que pode ser usado para identificar e caracterizar biomarcadores para aplicações médicas. Crédito:NIST
Cientistas do Instituto Nacional de Padrões e Tecnologia deram um passo mais perto de desenvolver os meios para um teste de sangue de diagnóstico rápido que pode fazer a varredura de milhares de marcadores de doenças e outros indicadores químicos de saúde. A equipe relata que aprendeu como decodificar os sinais elétricos gerados por um nanoporo - um "portão" com menos de 2 nanômetros de largura em uma membrana celular artificial.
Os nanoporos não são novos; por mais de uma década, os cientistas têm procurado usar um detector elétrico baseado em nanoporos para caracterizar o DNA de fita simples para aplicações de sequenciamento genético. Mais recentemente, Os cientistas do NIST voltaram sua atenção para o uso de nanoporos para identificar, quantificar e caracterizar cada um dos mais de 20, 000 proteínas que o corpo produz - uma capacidade que forneceria um instantâneo da saúde geral de um paciente em um determinado momento. Mas enquanto os nanoporos permitem que as moléculas entrem neles uma de cada vez, determinar por qual molécula individual específica acabou de passar não foi fácil.
Para resolver este problema, membros da equipe do NIST que anteriormente desenvolveu um método para distinguir o tamanho e a concentração de cada tipo de molécula que o nanopore admite, agora responderam à pergunta de como essas moléculas individuais interagem com o nanopore. Seu novo modelo teórico descreve a física e química de como o nanopore, na verdade, analisa uma molécula, um entendimento que irá promover o uso de nanoporos na área médica.
"Este trabalho nos traz um passo mais perto de perceber esses nanoporos como uma ferramenta de diagnóstico poderosa para a ciência médica, "diz Joseph Reiner, que realizou o trabalho com Joseph Robertson, e John Kasianowicz, todos da Divisão de Semicondutores Eletrônicos do NIST. "Acrescenta à 'Pedra de Roseta' que nos permitirá ler quais moléculas acabaram de passar por um nanoporo."
Usando seus novos métodos, a equipe foi capaz de modelar a interação de um tipo específico de molécula grande por meio da abertura de um nanoporo com grande precisão. As moléculas eram polietilenoglicol (PEG), um polímero bem conhecido que forma cadeias de comprimento variável.
"As cadeias de PEG podem ser muito longas, mas cada link é muito pequeno, "Kasianowicz diz." Foi um bom teste porque queríamos ver se o nanopore poderia diferenciar entre duas moléculas grandes quase idênticas que diferem em comprimento por apenas alguns átomos. "
O dispositivo da equipe foi capaz de distinguir facilmente entre cadeias de PEG de diferentes tamanhos, e o modelo que desenvolveram para descrever as interações PEG-nanopore está encorajando-os a pensar que, com mais esforço, os sensores minúsculos podem ser personalizados para medir muitas moléculas diferentes rapidamente. "Podemos construir uma série de muitos nanoporos, cada um criado para medir uma substância específica, "Kasianowicz diz." Porque cada nanoporo é tão pequeno, uma matriz com uma para cada proteína do corpo ainda seria minúscula. "