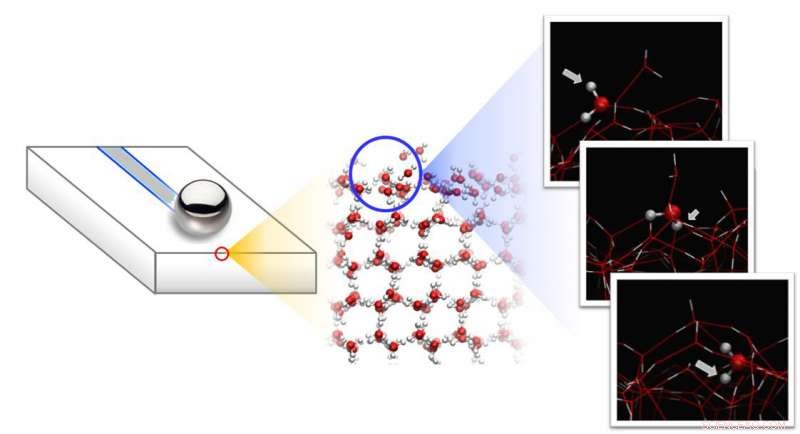
Nos experimentos, uma bola de aço desliza sobre a superfície do gelo, que consiste em moléculas de água móveis que se movem rapidamente e que estão apenas vagamente ligadas ao gelo subjacente. Crédito:Nagata / MPI-P
Esportes de inverno, como esqui, patinação de velocidade, patinação artística, e o curling requerem as superfícies escorregadias de gelo e neve. Embora o fato de que a superfície do gelo seja escorregadia seja amplamente reconhecido, está longe de ser totalmente compreendido. Em 1886 John Joly, um físico irlandês, ofereceu a primeira explicação científica para o baixo atrito no gelo; quando um objeto - isto é, um patim de gelo - toca a superfície do gelo, a pressão de contato local é tão alta que o gelo derrete, criando assim uma camada de água líquida que lubrifica o deslizamento. O consenso atual é que, embora a água líquida na superfície do gelo reduza o atrito de deslizamento no gelo, esta água líquida não é derretida por pressão, mas pelo calor de fricção produzido durante o deslizamento.
Uma equipe de pesquisadores liderada pelos irmãos Prof. Daniel Bonn da Universidade de Amsterdam e Prof. Mischa Bonn do MPI-P, agora demonstraram que o atrito no gelo é mais complexo do que se supôs. Por meio de experimentos de fricção macroscópica em temperaturas que variam de 0 ° C a -100 ° C, os pesquisadores mostram que - surpreendentemente - a superfície do gelo se transforma de uma superfície extremamente escorregadia em temperaturas típicas de esportes de inverno, para uma superfície com alto atrito a -100 ° C.
Para investigar a origem dessa escorregadia dependente da temperatura, os pesquisadores realizaram medições espectroscópicas do estado das moléculas de água na superfície, e comparou-os com simulações de dinâmica molecular (MD). Essa combinação de experimento e teoria revela que existem dois tipos de moléculas de água na superfície do gelo:moléculas de água que estão presas ao gelo subjacente (ligadas por três ligações de hidrogênio) e moléculas de água móveis que são ligadas por apenas duas ligações de hidrogênio. Essas moléculas de água móveis rolam continuamente sobre o gelo - como pequenas esferas - alimentadas por vibrações térmicas.
Conforme a temperatura aumenta, as duas espécies de moléculas de superfície são interconvertidas:o número de moléculas de água móveis é aumentado às custas das moléculas de água que são fixadas na superfície do gelo. Notavelmente, esta mudança impulsionada pela temperatura na mobilidade das moléculas de água superiores na superfície do gelo corresponde perfeitamente à dependência da temperatura da força de atrito medida:quanto maior a mobilidade na superfície, quanto menor o atrito e vice-versa. Os pesquisadores concluem, portanto, que - em vez de uma fina camada de água líquida no gelo - a alta mobilidade das moléculas de água da superfície é responsável pelo escorregamento do gelo.
Embora a mobilidade da superfície continue a aumentar até 0 ° C, esta não é a temperatura ideal para deslizar no gelo. Os experimentos mostram que o atrito é de fato mínimo a -7 ° C; a mesma temperatura exata é imposta nos rinques de patinação de velocidade. Os pesquisadores mostram que em temperaturas entre -7 ° C e 0 ° C, deslizar é mais difícil porque o gelo fica mais macio, fazendo com que o objeto deslizante se afunde mais profundamente no gelo.
Os resultados são publicados no Journal of Physical Chemistry Letters .