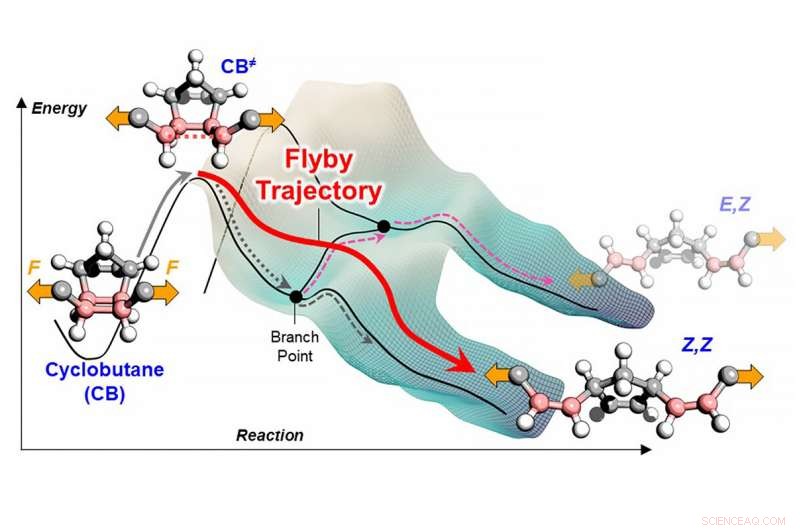
Uma ilustração que mostra o movimento de uma molécula através de uma superfície de energia potencial na forma como os caminhantes seguem o mapa de contorno de montanhas e vales ao longo de uma trilha. Quando uma força mecânica é aplicada, a energia aumenta e a molécula fica excitada, salta a barreira de energia inicial e tem energia suficiente para continuar sua "trajetória de voo" sobre a barreira de energia subsequente. Crédito:Yun Liu
Um novo estudo mostra que é possível usar a força mecânica para alterar deliberadamente as reações químicas e aumentar a seletividade química - um grande desafio do campo.
O estudo liderado pelo pesquisador da Universidade de Illinois Urbana-Champaign Jeffrey Moore e o químico da Universidade de Stanford Todd Martinezz demonstra como as forças mecânicas externas alteram os movimentos atômicos para manipular os resultados da reação. Os resultados do estudo são publicados na revista Ciência .
"Pensamos nas reações químicas como moléculas que se movem em uma superfície de energia potencial da mesma forma que os caminhantes seguem o mapa de contorno de montanhas e vales ao longo de uma trilha, "disse o autor principal Yun Liu, um pesquisador de pós-doutorado no grupo de pesquisa de Moore. “Uma montanha ao longo de um caminho de reação é uma barreira que precisa ser transposta antes que as moléculas possam descer até seu produto final. a altura relativa das barreiras controla qual caminho as moléculas provavelmente escolherão, permitindo que os químicos façam previsões sobre o que uma determinada reação química irá produzir - um resultado chamado seletividade. "
Os químicos tradicionalmente presumem que o movimento das moléculas - conhecido como "dinâmica molecular" - é governado por uma superfície de energia potencial. As moléculas se transformam por reações químicas que buscam o caminho que requer uma quantidade mínima de energia. Contudo, evidências emergentes mostram que as moléculas muitas vezes não têm tempo para amostrar a superfície, levando a desvios chamados de efeitos dinâmicos não estatísticos, disseram os pesquisadores.
Efeitos dinâmicos não estatísticos são observados em algumas reações comuns, como nitração de benzeno e reações de desidratação, "Liu disse." Apesar desses exemplos, As EQMs não capturaram totalmente a atenção dos químicos porque são difíceis de medir e não podem ser controladas para alterar os resultados da reação - a busca essencial da química. "
Liu desenvolveu um projeto experimental usando uma molécula de anel marcada com um isótopo de carbono-13 com duas cadeias de polímero anexadas. Liu colocou os polímeros em um recipiente de reação e aplicou uma força mecânica por meio de sonicação, que divide o anel em dois grupos separados.
"A molécula do anel pode se converter em um dos três produtos diferentes depois de ser rasgada, tornando-o um bom modelo para investigar EQMs, "Disse Liu." O rótulo 13-C nos permite rastrear e medir as mudanças químicas que ocorrem no anel, tornando-o distinto de milhares de outras ligações químicas no polímero. "
Liu levanta a hipótese de que, com a excitação da força mecânica, os átomos aquecem ao longo de direções de reação específicas, ao invés de seguir as direções moldadas pela superfície de energia potencial. Os pesquisadores chamaram esse desvio do conceito convencional de reações químicas de "trajetória de sobrevôo".
"Usando o exemplo de caminhada, a hipótese equivale a dizer que o caminhante simplesmente decidiu não seguir o mapa, "Liu disse." Em vez disso, o alpinista estava animado o suficiente para pular em uma asa-delta e voar entre as colinas durante a descida. Como resultado, a direção em que as moléculas se movem torna-se dependente de seu salto inicial, em vez da altura da barreira subsequente. "
Liu realizou vários experimentos demonstrando a capacidade de ajuste da trajetória de sobrevôo, aumentando a força mecânica de modo que a reação possa cada vez mais superar as barreiras. Idealmente, os pesquisadores podem transformar uma reação não seletiva em uma altamente seletiva, onde quaisquer produtos colaterais formados são indetectáveis.
Para apoiar a descoberta experimental, O estudante de graduação da Stanford University Soren Holm coletou 10, 000, 000 geometrias computadas para construir um modelo teórico da superfície de energia potencial e, em seguida, extrair a velocidade das trajetórias de reação sob a presença de força mecânica.
"Descobrimos que as trajetórias iniciais não diminuem ao passar pelas barreiras, "Liu disse.
Em outras palavras, barreiras são ultrapassadas em vez de superadas, que deveria ter desacelerado a taxa de reação química, disseram os pesquisadores. Hora extra, as moléculas esfriam, e as trajetórias subsequentes seguem o caminho de energia mínimo inicialmente previsto.
"Nossas descobertas darão aos pesquisadores uma compreensão mais completa de como a força pode alterar o curso das reações químicas para aumentar a eficiência da produção, "Moore disse." É outra ferramenta em nossa caixa de ferramentas para fazer as coisas que usamos todos os dias. "
The National Science Foundation, o Escritório de Pesquisa do Exército, a Fundação Dr. Leni Schoninger e a Deutsche Forschungsgemeinschaft apoiaram esta pesquisa.
Moore é o diretor do Instituto Beckman de Ciência e Tecnologia Avançada, um professor de química e ciências de materiais e engenharia e é afiliado ao Center for Advanced Study, o Laboratório de Pesquisa de Materiais, o Carle Illinois College of Medicine, o Instituto Carl R. Woese de Biologia Genômica e o Centro de Ciências Sociais e Comportamentais.