Pesquisadores descobrem um caminho eficaz para converter dióxido de carbono em etileno
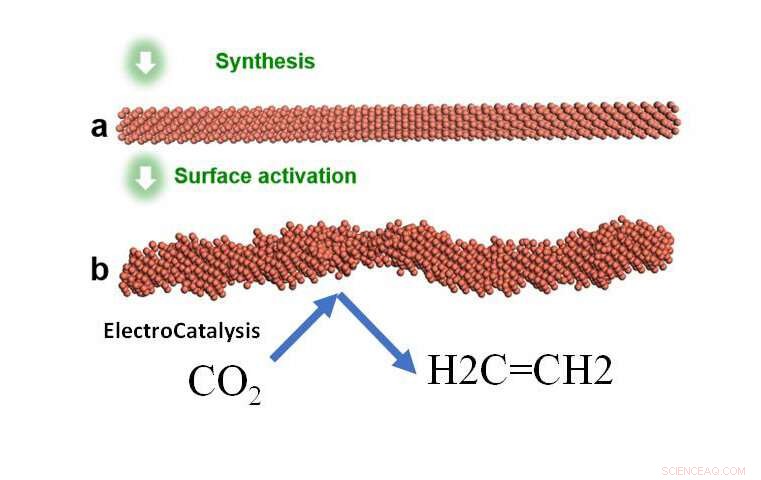 p Ilustração do sistema de eletrocatálise que sintetizou o nanofio liso e o ativou aplicando uma voltagem para obter a superfície áspera escalonada que é altamente seletiva para a redução de CO2 em etileno. Crédito:Yu Huang e William A. Goddard III
p Ilustração do sistema de eletrocatálise que sintetizou o nanofio liso e o ativou aplicando uma voltagem para obter a superfície áspera escalonada que é altamente seletiva para a redução de CO2 em etileno. Crédito:Yu Huang e William A. Goddard III
p Uma equipe de pesquisa da Caltech e da Escola de Engenharia da UCLA Samueli demonstrou uma maneira promissora de converter dióxido de carbono em etileno, um importante produto químico usado para produzir plásticos, solventes, cosméticos e outros produtos importantes em todo o mundo. p Os cientistas desenvolveram fios de cobre em nanoescala com superfícies de formato especial para catalisar uma reação química que reduz as emissões de gases de efeito estufa enquanto gera etileno - um produto químico valioso simultaneamente. Estudos computacionais da reação mostram que o catalisador moldado favorece a produção de etileno em vez de hidrogênio ou metano. Um estudo detalhando o avanço foi publicado em
Catálise Natural .
p "Estamos à beira da exaustão dos combustíveis fósseis, juntamente com os desafios da mudança climática global, "disse Yu Huang, o co-autor do estudo, e professor de ciência de materiais e engenharia na UCLA. "O desenvolvimento de materiais que podem transformar eficientemente gases de efeito estufa em combustíveis de valor agregado e matérias-primas químicas é uma etapa crítica para mitigar o aquecimento global enquanto evita a extração de combustíveis fósseis cada vez mais limitados. Este experimento integrado e análise teórica apresentam um caminho sustentável para o aumento do dióxido de carbono e utilização."
p Atualmente, o eteno tem uma produção anual global de 158 milhões de toneladas. Muito disso é transformado em polietileno, que é usado em embalagens de plástico. O etileno é processado a partir de hidrocarbonetos, como o gás natural.
p "A ideia de usar cobre para catalisar essa reação existe há muito tempo, mas a chave é acelerar a taxa para que seja rápida o suficiente para a produção industrial, "disse William A. Goddard III, o co-autor do estudo e o professor de química Charles e Mary Ferkel da Caltech, Ciência de materiais, e Física Aplicada. “Este estudo mostra um caminho sólido em direção a essa marca, com potencial para transformar a produção de etileno em uma indústria mais verde usando CO
2 isso, de outra forma, acabaria na atmosfera. "
p Usando cobre para iniciar o dióxido de carbono (CO
2 ) redução na reação de etileno (C
2 H
4 ) sofreu dois ataques contra ele. Primeiro, a reação química inicial também produziu hidrogênio e metano - ambos indesejáveis na produção industrial. Segundo, tentativas anteriores que resultaram na produção de eteno não duraram muito, com a eficiência de conversão diminuindo conforme o sistema continuava em execução.
p Para superar esses dois obstáculos, os pesquisadores se concentraram no projeto dos nanofios de cobre com "degraus" altamente ativos - semelhantes a um conjunto de escadas dispostas em escala atômica. Uma descoberta intrigante deste estudo colaborativo é que este padrão de etapas nas superfícies dos nanofios permaneceu estável sob as condições de reação, ao contrário da crença geral de que essas características de alta energia se suavizariam. Esta é a chave para a durabilidade e seletividade do sistema na produção de etileno, em vez de outros produtos finais.
p A equipe demonstrou uma taxa de conversão de dióxido de carbono em etileno superior a 70%, muito mais eficiente do que os designs anteriores, que rendeu pelo menos 10% menos nas mesmas condições. O novo sistema funcionou por 200 horas, com pouca mudança na eficiência de conversão, um grande avanço para catalisadores à base de cobre. Além disso, a compreensão abrangente da relação estrutura-função ilustrou uma nova perspectiva para projetar CO altamente ativo e durável
2 catalisador de redução em ação.
p Huang e Goddard são colaboradores frequentes há muitos anos, com o grupo de pesquisa de Goddard enfocando as razões teóricas que sustentam as reações químicas, enquanto o grupo de Huang criou novos materiais e conduziu experimentos. O autor principal do artigo é Chungseok Choi, estudante de graduação em ciência de materiais e engenharia na UCLA Samueli e membro do laboratório de Huang.
