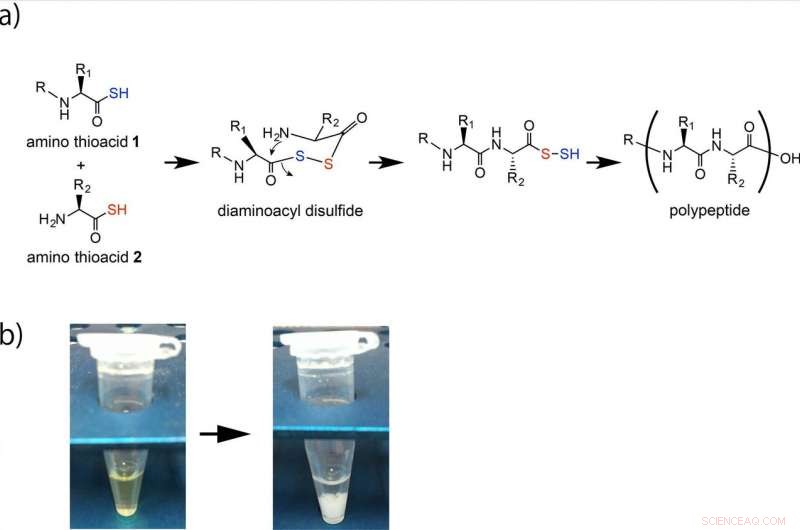
Formação de polipeptídeos pela reação oxidativa de aminotioácidos. (a) Os aminoácidos 1 e 2 são acoplados por meio de um intermediário de diaminoacil dissulfeto e a subsequente formação de amida intramolecular gera uma ligação alfa-amida. O minério de ferro ou Fe2O3 em solução ácida acelera a formação desse polipeptídeo. O desempenho repetitivo desta reação produz o polipeptídeo. (b) O polipeptídeo é formado como um precipitado branco. Crédito:Universidade de Osaka
Os principais constituintes das células, tecido, órgãos, e organismos inteiros são proteínas, que são construídos pela adição de aminoácidos um após o outro para formar longas cadeias de proteínas chamadas polipeptídeos. Embora as células vivas tenham maquinário avançado que pode alcançar essa extensão da cadeia com velocidade e precisão surpreendentes, os esforços para imitar essa reação no laboratório a fim de criar produtos peptídicos naturais ou drogas peptídicas permaneceram rudes e trabalhosos em comparação.
Usando variantes de aminoácidos chamados aminotioácidos, uma equipe da Universidade de Osaka superou essas dificuldades para alcançar a extensão precisa e simples das cadeias de peptídeos em uma reação rápida. Trabalho deles, publicado no jornal Bioquímica , também sugere que, bilhões de anos atrás, este mecanismo químico específico poderia ter permitido o aparecimento de uma abundância de moléculas maiores e mais complexas, potencialmente fornecendo as condições das quais a vida eventualmente surgiu.
Neste estudo, a equipe se concentrou em melhorar os esforços anteriores para sintetizar polipeptídeos artificialmente, em que um grande obstáculo era a necessidade de incluir grupos protetores. Esses grupos de proteção são adicionados a grupos funcionais dentro de uma molécula para garantir que uma reação subsequente seja específica. Contudo, eles exigem vários estágios de reação a serem realizados, o que torna o procedimento ineficiente.
"Em nossos esforços para melhorar a formação de ligações peptídicas artificiais, em vez de focar em aminoácidos, em vez disso, olhamos para os aminoácidos, que incluem um átomo de enxofre, "Yasuhiro Kajihara diz." Começamos com a versão aminotioácido da fenilalanina como monômero, e sob uma reação que durou apenas cinco minutos descobriu que cadeias de peptídeos contendo duas a cinco fenilalaninas se formaram. Uma análise alternativa revelou cadeias de até 12 fenilalaninas. "
Uma imagem da formação de polipeptídeos por aminotioácidos na superfície do minério de ferro em solução ácida. Crédito:Universidade de Osaka
A equipe então mostrou que a extensão da cadeia peptídica ocorreu com misturas de amino tioácidos e também apenas em condições ácidas, o que sugeriu que a oxidação era a chave para o mecanismo envolvido. A equipe confirmou isso ao caracterizar a reação, e também mostrou que envolvia um intermediário de reação único, que garantiu que o produto pretendido foi gerado com precisão.
"Dado que a extensão de aminoácidos regulares em cadeias é um fator chave para a vida, nos perguntamos se, bilhões de anos atrás, aminotioácidos poderiam ter atuado como um precursor da química mais complexa que levou ao desenvolvimento da vida senciente, tendo em vista sua rápida e simples incorporação em cadeias, "O autor principal Ryo Okamoto diz." Descobrimos que a reação de oligomerização também ocorreu sob condições químicas semelhantes às da Terra antes do surgimento da vida, usando componentes de reação, como minério de ferro e ácido sulfúrico, que poderia ter sido gerado a partir de gás vulcânico. "
O trabalho da equipe, portanto, fornece não apenas uma ferramenta de laboratório eficiente para uma variedade de aplicações práticas, mas também um vislumbre potencial da química a partir da qual a vida começou.