Dissolução seletiva de ouro elementar de fontes multi-metal em soluções orgânicas
 p Crédito:Angewandte Chemie
p Crédito:Angewandte Chemie
p "Mineração urbana", a reciclagem de metais preciosos de aparelhos eletrônicos, torna-se cada vez mais importante, embora os processos que são eficientes e ambientalmente benignos ainda sejam escassos. Uma equipe internacional de cientistas agora examinou mais profundamente a dissolução do ouro, em particular, como compostos orgânicos contendo tiol ajudam a dissolver o ouro elementar. Seu estudo publicado na revista
Angewandte Chemie propõe seletiva, velozes, e processos convenientes de lixiviação de ouro auxiliados por tiol. p A maneira tradicional de reciclar "resíduos" de ouro está derretendo:ouro dental e joias podem ser reciclados em quase 100%. Reciclagem de metais preciosos em smartphones, computadores, e outros aparelhos eletrônicos são muito mais difíceis, e a cotação de recuperação ainda é baixa. Apesar de sua abundância em dispositivos eletrônicos, seu conteúdo relativo ainda é muito baixo para permitir uma mineração urbana realmente econômica.
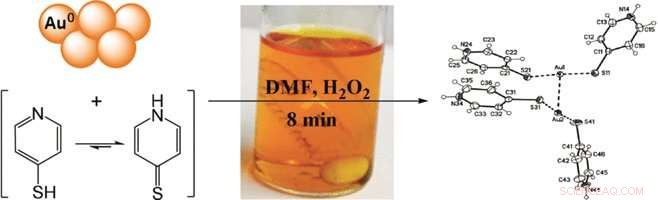
p O método tradicional de mineração de ouro é a lixiviação de cianeto hidrometalúrgico, que produz uma grande quantidade de resíduos perigosos, embora seja relativamente não seletivo. Conceitos mais recentes baseiam-se na complexação de ouro em soluções orgânicas porque forma complexos solúveis com reagentes contendo enxofre. Contudo, os processos devem ser viáveis em larga escala e ainda evitar compostos tóxicos ou perigosos. Agora, Timo Repo da Universidade de Helsinque, Finlândia, e seus colegas examinaram mais profundamente os detalhes da extração seletiva de ouro em solução orgânica. Eles propõem um método eficiente de recuperação de ouro a partir de resíduos eletrônicos com piridinetióis e peróxido de hidrogênio como reagentes, a dimetilformamida química como solvente orgânico, e, opcionalmente, enxofre elementar para reduzir a carga de reagente.
p Piridinotiol é piridina, um anel aromático contendo nitrogênio, com um grupo tiol, SH, adicionado ao seu anel. O reagente não se liga apenas ao ouro elementar para formar complexos solúveis, mas o complexo também tem uma estrutura linear favorável formada por duas moléculas de piridinotiol em cada lado do átomo de ouro. Após a oxidação, ele se transforma em um produto contendo ouro catiônico estável em solução orgânica. Esta formação complexa com dois ligantes é uma especialidade de ouro, favorecendo a energética de dissolução e oxidação. De acordo, os autores relataram a dissolução quase quantitativa do ouro do pó, filme, ou placas eletrônicas após 20 minutos de tempo de extração.
p Mas como a dissolução do ouro pode ser distinguida da de outros metais preciosos? Em contraste com o ouro tendo uma oxidação de um elétron, platina e paládio requerem oxidações de dois elétrons e, portanto, não são acessíveis com este método. Em contraste, tanto o cobre quanto a prata formam complexos com piridinetióis, embora não seja tão eficaz quanto o ouro. Portanto, antes de dissolver o ouro da região do "dedo de ouro" em uma placa de circuito impresso, os cientistas primeiro extraíram cobre e prata com soluções contendo amônia e sulfato, que são métodos estabelecidos.
p Olhando para o mecanismo exato de dissolução de ouro assistida por tiol, os cientistas descobriram uma variedade surpreendentemente alta de produtos colaterais contendo enxofre. Alguns deles pareciam ser cruciais para o prosseguimento da reação de oxidação, por exemplo
8 , uma forma comum de enxofre elementar. Isso também provou ser uma vantagem:ao adicionar S externo
8 , a carga de ligante pode ser reduzida, relataram os autores. Seu método de extração pode marcar uma nova base para uma mineração urbana mais eficiente.
