Crédito:Wiley
As reações de transferência de oxigênio e elétrons acopladas que usam cofatores são reações enzimáticas de importância crucial para todas as formas de vida, desde bactérias até vertebrados. No European Journal of Inorganic Chemistry , os cientistas introduziram um modelo para a enzima sulfito oxidase. É baseado em um complexo de molibdênio cujos ligantes especiais podem ser oxidados para permitir o acoplamento da transferência de oxigênio a um substrato com uma transferência de elétrons intramolecular. Os intermediários contendo molibdênio (V) -ion desempenham um papel crítico.
Muitas enzimas não funcionam sozinhas; eles requerem cofatores - componentes não proteicos que desempenham um papel na transferência de elétrons. Muitas vezes envolvem íons de metal, como o ferro nos citocromos ou o oligoelemento molibdênio, que é encontrado em oxotransferases de molibdênio, enzimas que transferem átomos de oxigênio para substratos. Um importante representante deste último é a sulfito oxidase, que oxida o sulfito tóxico para produzir sulfato. A transferência de oxigênio envolve uma mudança no estado de oxidação do molibdênio de tetravalente (MoIV) para pentavalente (MoV). Os elétrons envolvidos são removidos por meio de citocromos e usados para a produção de ATP. O molibdênio pentavalente (MoV) parece ser um intermediário na reação.
Os pesquisadores que trabalham com Katja Heinze na Universidade de Mainz desenvolveram agora uma abordagem conceitual para estabilizar e caracterizar espectroscopicamente os intermediários previstos nas reações de oxotransferases contendo Mo usando sistemas modelo. Eles usam um método que também é usado no controle de catalisadores:eles conectam uma "chave" molecular com um estado de oxidação controlável.
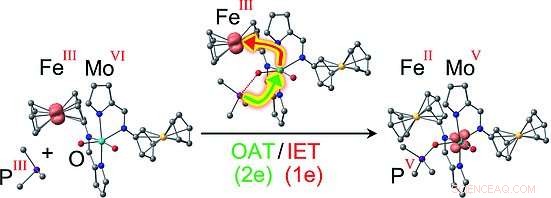
Os pesquisadores optaram por usar o par redox ferroceno / ferrocênio, em que um átomo de ferro está imprensado entre dois carregados negativamente, aromático, anéis de carbono de cinco membros. O íon de ferro pode alternar entre um estado com uma carga positiva dupla (FeII, ferroceno) e um triplo com carga positiva, estado oxidado (FeIII, ferrocênio). Isso é análogo aos cofatores de citocromo que ocorrem naturalmente, que também pode conter FeII ou FeIII. Os pesquisadores anexaram duas dessas "chaves" de ferroceno / ferrocênio a um complexo de molibdênio como um modelo para o centro ativo de uma sulfito oxidase. O molibdênio está no estado de oxidação VI e possui dois átomos de oxigênio ligados por ligações duplas. A reação com um fosfano orgânico (uma molécula de hidrocarboneto de fósforo) como um substrato modelo aceitador de oxigênio ocorre em taxas variáveis, dependendo das cobranças nos "interruptores", porque o status redox dos substituintes ferrocenyl modula as barreiras de energia para certos intermediários. Isso resulta em uma variedade de adutos entre o complexo de Mo e o fosfano.
As versões mais interessantes são aquelas com dois íons FeIII ou um íon FeII e um íon FeIII:Nestes casos, o mecanismo não é mais uma simples transferência de um átomo de oxigênio para o substrato, quanto à versão FeII / FeII. Em vez disso, é acoplado a uma transferência de elétrons intramolecular, possivelmente conceitualmente semelhante ao das sulfito oxidases naturais. Durante a reação de transferência de oxigênio, um elétron é transferido do molibdênio para um dos íons FeIII, resultando em uma distribuição de carga de FeII FeIII MoV ou FeII FeII MoV. Para a última versão, os pesquisadores foram capazes de usar espectroscopia de ressonância de spin eletrônico para detectar inequivocamente o intermediário MoV FeII FeII MoV com o substrato oxidado (o produto) ainda ligado a ele. O acoplamento da transferência de oxigênio a uma transferência de elétrons intermolecular reduz a barreira de ativação para esta etapa de reação e simultaneamente estabiliza o intermediário MoV, conforme previsto pelos modelos de computador.
Os pesquisadores propõem o uso deste novo sistema como modelo para as etapas de transferência de átomos de oxigênio e transferência intramolecular de elétrons em sulfito oxidases, e espero usar este novo conceito para desenvolver análogos para futuras reações enzimáticas com transferência de elétrons acoplada. No futuro, também parece possível estender este conceito para reações catalíticas comutáveis que não possuem protótipo natural.