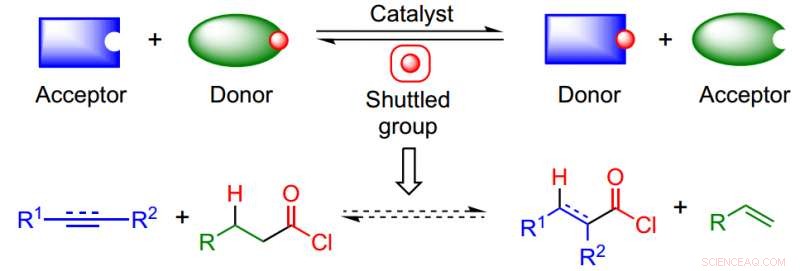
A abordagem aproveita a vantagem de um processo de catálise isodésmica para eludir a necessidade de CO e HCl e superar o desafio termodinâmico de fazer produtos altamente reativos. Crédito: Química da Natureza (2017). DOI:10.1038 / nchem.2798
(Phys.org) —A síntese de derivados de ácido carboxílico de compostos de carbono insaturados é importante para fazer produtos químicos usados em produtos farmacêuticos, cosméticos, polímeros, e agroquímicos. Na indústria, essa reação é feita usando monóxido de carbono de alta pressão junto com o catalisador apropriado para o trabalho. Embora isso possa ser possível em certas instalações, o uso de um gás venenoso não é viável no ambiente de laboratório. Adicionalmente, porque essas reações muitas vezes requerem um catalisador feito sob medida, o processo é limitado apenas aos substratos que funcionam com o catalisador.
Pesquisadores do Instituto Max Planck desenvolveram uma síntese que é muito mais ampla em escopo e evita o uso de CO de alta pressão e gás HCl corrosivo. Xianjie Fang, Bastien Cacherat, e Bill Morandi desenvolveu uma nova síntese em um único recipiente que produz uma variedade de ácidos carboxílicos, bem como amidas e tioésteres. Sua síntese emprega um vaivém catalítico que doa o CO e o HCl necessários para produzir um intermediário de cloreto de ácido que é então convertido no produto desejado. O trabalho deles aparece em Química da Natureza .
A catálise do vaivém elimina a necessidade de usar reagentes perigosos e abre a porta para o uso de nucleófilos que não eram acessíveis sob outras condições de reação (ou seja, Carbonilação Reppe) De acordo com o Dr. Morandi, "O catalisador atua efetivamente como um lançador para o transporte de um grupo químico entre uma molécula (doadora) e outra molécula (aceitadora) de forma reversível."
Nesse artigo, os autores combinaram um doador de cloreto de ácido e um substrato insaturado para produzir o cloreto de ácido desejado que pode então ser convertido em uma ampla gama de grupos funcionais úteis. A nave deles era Pd / xantphos, um sistema catalítico que tem sido usado em outros tipos de reações de alceno.
A chave para sua síntese era encontrar uma molécula doadora de CO e HCl apropriada. Como uma reação modelo, Fang et al. usou ciclododecina, um alcino interno, e tentaram vários cloretos de ácido alifático de baixo peso molecular como suas moléculas doadoras. Eles determinaram que o cloreto de butiril era o seu melhor candidato porque é barato, tem um baixo peso molecular, e tem boa reatividade.
Eles então investigaram o escopo de seu mecanismo de reação. Vários dos alcinos internos que eles investigaram requeriam apenas um pouco mais de um equivalente de cloreto de butirila e produziram o produto de cloreto de ácido desejado com bons rendimentos. Além disso, porque a reação é sensível aos efeitos estéricos, os produtos apresentavam excesso de um produto da região e reagiam seletivamente na posição distal nos casos em que havia mais de uma opção de reação.
As condições de reação também funcionaram para alcinos terminais. Para esta reação, cerca de quatro equivalentes de cloreto de butirila foram necessários e o isômero ramificado foi isolado da reação para dar o produto desejado com bom rendimento. Os autores observaram que foram capazes de isolar produtos de acrilato de alquila, que são compostos importantes para a química de polímeros. Eles também testaram sua reação com halogênios, álcoois protegidos, ésteres, uma cetona, um nitrilo, e ftalimidas, todos os quais foram bem tolerados nesta reação.
Fang et al. também testou como essa reação se saiu com os alcenos. Eles produziram cloretos de ácido de bicicleta a partir de alcenos distendidos com bons rendimentos. Os alcenos terminais deram o cloreto de ácido correspondente em rendimentos adequados.
A próxima etapa em seu procedimento foi fazer uma síntese em um único recipiente, convertendo o cloreto de ácido no ácido carboxílico correspondente, tioester, ou amida. Eles começaram observando os nucleófilos que normalmente são inacessíveis quando feitos com as reações relatadas anteriormente. Estes incluíam um álcool terciário bulk e tocoferol. Eles também testaram o indol e um tiol terciário. Eles também foram capazes de conjugar cinchonina e estrona, duas moléculas bioativas.
Finalmente, sua síntese em um só vaso foi testada para ver se poderia ser usada para fazer outros compostos de carbonila. Isso exigia o uso de diferentes substratos iniciais e um segundo catalisador. Estes incluíram reações de Friedel-Crafts, bem como outras reações de acoplamento para produzir cetonas.
Em relação às implicações mais amplas de seu trabalho, Dr. Morandi disse que "este trabalho demonstra que a catálise do ônibus espacial não é apenas uma abordagem valiosa para evitar o uso de gases tóxicos, mas também uma ferramenta poderosa para descobrir nova reatividade que é difícil de obter de outra forma "
© 2017 Phys.org