A plataforma de nanopartículas GPS fornece com precisão carga terapêutica às células cancerígenas
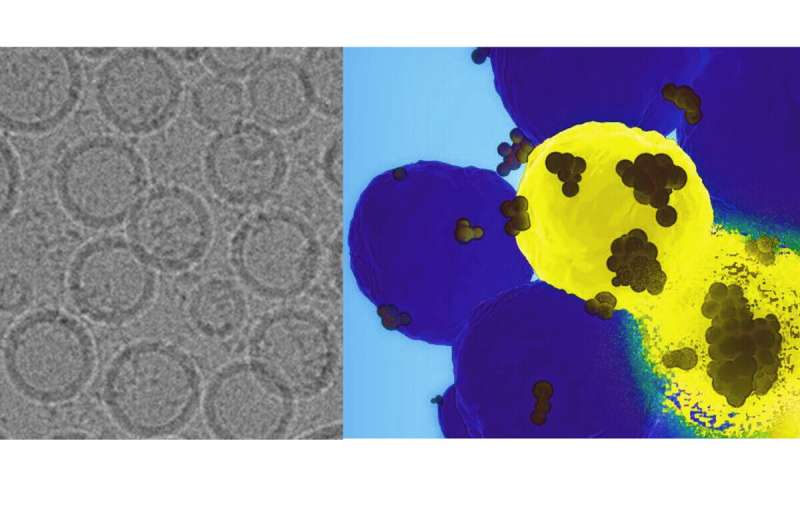 À esquerda está uma imagem microscópica eletrônica das nanopartículas projetadas pela equipe liderada por pesquisadores da Penn State. À direita, as nanopartículas, mostradas como pontos pretos, encontram as células basais do câncer de mama em amarelo e fornecem as ferramentas de edição genética. A célula em desintegração demonstra o poder destrutivo da terapia administrada pela nanopartícula. Crédito:Dipanjan Pan/Penn State
À esquerda está uma imagem microscópica eletrônica das nanopartículas projetadas pela equipe liderada por pesquisadores da Penn State. À direita, as nanopartículas, mostradas como pontos pretos, encontram as células basais do câncer de mama em amarelo e fornecem as ferramentas de edição genética. A célula em desintegração demonstra o poder destrutivo da terapia administrada pela nanopartícula. Crédito:Dipanjan Pan/Penn State Uma "nanopartícula GPS" recém-desenvolvida, injetada por via intravenosa, pode atingir as células cancerosas para fornecer um impacto genético à proteína implicada no crescimento e disseminação do tumor, de acordo com pesquisadores da Penn State. Eles testaram a sua abordagem em linhas celulares humanas e em ratos para derrubar eficazmente um gene causador de cancro, relatando que a técnica pode potencialmente oferecer um tratamento mais preciso e eficaz para cancros da mama do tipo basal, notoriamente difíceis de tratar.
Eles publicaram seu trabalho no ACS Nano . Eles também entraram com um pedido provisório de patente da tecnologia descrita no estudo.
"Desenvolvemos uma nanopartícula GPS que pode encontrar o local onde é necessária", disse o autor correspondente Dipanjan Pan, professor catedrático Dorothy Foehr Huck &J. Lloyd Huck em Nanomedicina e professor de engenharia nuclear e de ciência e engenharia de materiais na Penn State .
"Uma vez lá - e somente lá - ele pode fornecer proteínas de edição genética para evitar que as células cancerígenas se espalhem. Foi uma tarefa difícil, mas mostramos que o sistema funciona para cânceres de mama do tipo basal."
Semelhante aos cancros da mama triplo-negativos, os cancros da mama do tipo basal podem ser menos prevalentes do que outros cancros da mama, mas podem ser muito mais difíceis de tratar, em grande parte porque não possuem os três alvos terapêuticos encontrados noutros cancros da mama. Eles também tendem a ser tumores agressivos, de crescimento rápido e eliminação de células que se espalham por outras partes do corpo. Essas células podem semear tumores adicionais, um processo chamado metástase.
“A metástase é um enorme desafio, especialmente com cancros como o cancro da mama triplo-negativo e do tipo basal”, disse Pan. “O cancro pode ser difícil de detectar e não aparece durante uma mamografia de rotina, e afecta principalmente a população mais jovem ou afro-americana que pode ainda não estar a receber cuidados preventivos. necessidade clínica não atendida de tratamentos mais eficazes quando o câncer não é detectado precocemente”.
A equipe fabricou uma nanopartícula de cavalo de Tróia, disfarçando-a com moléculas gordurosas especialmente projetadas que se parecem com lipídios naturais e enchendo-a de moléculas CRISPR-Cas9. Estas moléculas podem atingir o material genético de uma célula, identificar um gene específico e derrubá-lo ou torná-lo ineficaz. Neste caso, o sistema teve como alvo a caixa de forquilha humana c1 (FOXC1), que está envolvida na instigação da metástase.
Pan descreveu os lipídios projetados como “zwitteriônicos”, o que significa que eles têm carga quase neutra na casca da nanopartícula. Isto evita que o sistema imunitário do corpo ataque a nanopartícula – porque está disfarçada como uma molécula normal e não ameaçadora – e pode ajudar a libertar a carga útil, mas apenas quando os lípidos reconhecem o ambiente de baixo pH da célula cancerosa.
Para garantir que os lipídios só seriam ativados nesse pH baixo, os pesquisadores os projetaram para mudar suas cargas para positivas assim que entrassem no microambiente tumoral mais ácido, desencadeando a liberação da carga útil.
Mas o corpo é um lugar vasto, então como poderiam os investigadores garantir que a carga útil do CRISPR-Cas9 chegasse ao alvo correto? Para garantir que a nanopartícula se ligasse às células certas, eles anexaram uma molécula de adesão de células epiteliais (EpCAM), que é conhecida por se ligar a células de cancro da mama do tipo basal.
"Ninguém jamais tentou atingir uma célula cancerígena semelhante à da mama, semelhante à basal, com um sistema de entrega responsivo ao contexto que possa derrubar geneticamente o gene de interesse", disse Pan. "Somos os primeiros a mostrar que isso pode ser feito."
Outros desenvolveram sistemas de entrega viral, sequestrando uma partícula de vírus para levar o tratamento às células, e sistemas de entrega não virais, usando nanopartículas. A diferença, disse Pan, para a abordagem de sua equipe é o lipídio de superfície projetado para responder apenas no ambiente alvo, o que reduz o potencial de distribuição fora do alvo e danos às células saudáveis.
Além disso, acrescentou, como o corpo não considera os lípidos uma ameaça, há menos hipóteses de uma resposta imunitária, o que foi validado nas suas experiências.
A equipe primeiro testou a abordagem em células humanas de câncer de mama triplo-negativas, validando que a nanopartícula implantaria o sistema CRISPR/Cas9 no ambiente correto. Eles confirmaram que a nanopartícula poderia chegar a um tumor em um modelo de camundongo, implantar o sistema e derrubar com sucesso o FOXC1.
Em seguida, disse Pan, os pesquisadores planejam continuar testando a plataforma de nanopartículas com o objetivo final de aplicá-la clinicamente em humanos.
“Também estamos explorando outras formas de aplicar a tecnologia da plataforma”, disse Pan. "Podemos personalizar as moléculas na superfície, a carga útil que ela carrega, e usá-la para estimular a cura em outras áreas. Há muito potencial nesta plataforma."
