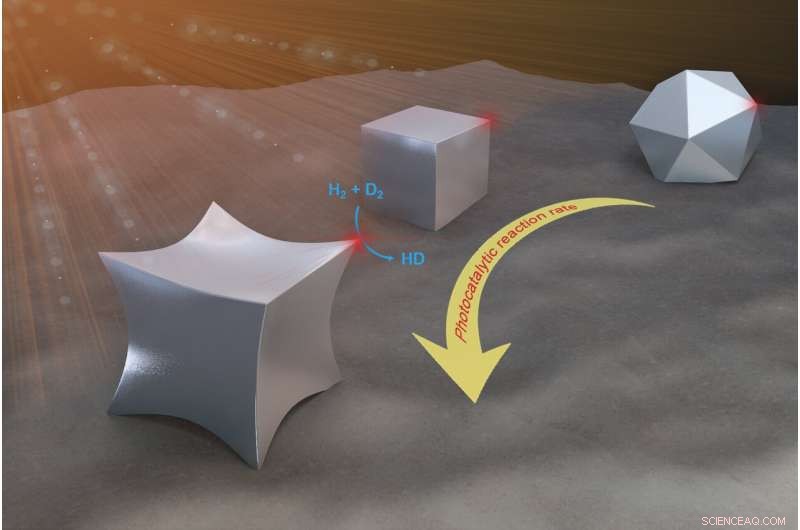
 p Um estudo de nanocatalisadores de alumínio pelo Laboratório de Nanofotônica da Rice University descobriu que os octópodes (à esquerda), partículas de seis lados com cantos bem pontiagudos, teve uma taxa de reação cinco vezes maior do que os nanocubos (centro) e 10 vezes maior do que os nanocristais de 14 lados. Crédito:Lin Yuan / Rice University
p Um estudo de nanocatalisadores de alumínio pelo Laboratório de Nanofotônica da Rice University descobriu que os octópodes (à esquerda), partículas de seis lados com cantos bem pontiagudos, teve uma taxa de reação cinco vezes maior do que os nanocubos (centro) e 10 vezes maior do que os nanocristais de 14 lados. Crédito:Lin Yuan / Rice University
p Os pontos são importantes ao projetar nanopartículas que geram reações químicas importantes usando o poder da luz. p Pesquisadores do Laboratório de Nanofotônica da Rice University (LANP) sabem há muito tempo que a forma de uma nanopartícula afeta como ela interage com a luz, e seu último estudo mostra como a forma afeta a capacidade de uma partícula de usar a luz para catalisar reações químicas importantes.
p Em um estudo comparativo, Os alunos de graduação do LANP Lin Yuan e Minhan Lou e seus colegas estudaram nanopartículas de alumínio com propriedades ópticas idênticas, mas formatos diferentes. O mais arredondado teve 14 lados e 24 pontos contundentes. Outro era em forma de cubo, com seis lados e oito cantos de 90 graus. O terceiro, que a equipe apelidou de "octopod, "também tinha seis lados, mas cada um de seus oito cantos terminava em uma ponta pontiaguda.
p Todas as três variedades têm a capacidade de capturar energia da luz e liberá-la periodicamente na forma de elétrons quentes superenergéticos que podem acelerar as reações catalíticas. Yuan, um químico do grupo de pesquisa da diretora do LANP Naomi Halas, conduziu experimentos para ver o quão bem cada uma das partículas funcionou como fotocatalisadores para a reação de dissociação de hidrogênio. Os testes mostraram que os octópodes tiveram uma taxa de reação 10 vezes maior do que os nanocristais de 14 lados e cinco vezes maior do que os nanocubos. Octopods também tiveram uma energia de ativação aparente mais baixa, cerca de 45% menor do que os nanocubos e 49% menor do que os nanocristais.
p "Os experimentos demonstraram que cantos mais agudos aumentaram a eficiência, "disse Yuan, co-autor do estudo, que é publicado na revista American Chemical Society
ACS Nano. “Para os polvos, o ângulo dos cantos é de cerca de 60 graus, em comparação com 90 graus para os cubos e mais pontos arredondados nos nanocristais. Portanto, quanto menor o ângulo, quanto maior o aumento na eficiência da reação. Mas o quão pequeno o ângulo pode ser é limitado pela síntese química. São cristais únicos que preferem certas estruturas. Você não pode tornar infinitamente mais nitidez. "
p Lou, um físico e co-autor de estudos no grupo de pesquisa de Peter Nordlander, do LANP, verificaram os resultados dos experimentos catalíticos desenvolvendo um modelo teórico do processo de transferência de energia de elétrons quentes entre as nanopartículas de alumínio ativadas por luz e as moléculas de hidrogênio.
p "Inserimos o comprimento de onda da luz e a forma das partículas, "Lou disse." Usando esses dois aspectos, podemos prever com precisão qual forma produzirá o melhor catalisador. "
p O trabalho é parte de um esforço contínuo de química verde da LANP para desenvolver nanocatalisadores ativados por luz comercialmente viáveis que podem inserir energia em reações químicas com precisão cirúrgica. LANP já demonstrou catalisadores para produção de etileno e gás de síntese, a divisão da amônia para produzir hidrogênio combustível e para quebrar "substâncias químicas eternas".
p "Este estudo mostra que a forma do fotocatalisador é outro elemento de design que os engenheiros podem usar para criar fotocatalisadores com taxas de reação mais altas e barreiras de ativação mais baixas, "disse Halas, Stanley C. Moore, professor de Engenharia Elétrica e da Computação de Rice, diretor do Instituto Smalley-Curl de Rice e professor de química, Bioengenharia, física e astronomia, e ciência de materiais e nanoengenharia.
