Nanopartículas magnéticas quebram a barreira da capacidade de purificação de anticorpos
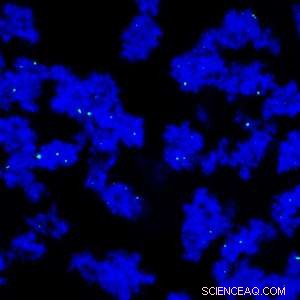 p Uma nova técnica de separação usa nanopartículas magnéticas revestidas com amido (verde) e polietilenoglicol para purificar anticorpos monoclonais (azul). Crédito:© 2013 Elsevier
p Uma nova técnica de separação usa nanopartículas magnéticas revestidas com amido (verde) e polietilenoglicol para purificar anticorpos monoclonais (azul). Crédito:© 2013 Elsevier
p Os anticorpos monoclonais representam o maior e mais rápido segmento da biofarma internacional. Embora esses agentes terapêuticos sejam uma bênção para a saúde global, restrições de produtividade representam um sério desafio para os fabricantes que buscam fazer quantidades suficientes para aplicações terapêuticas. Agora, Os pesquisadores do A * STAR desenvolveram um método de alta capacidade para purificar anticorpos monoclonais que usa nanopartículas magnéticas e também introduz novas condições operacionais. p Atualmente, anticorpos terapêuticos são geralmente purificados por uma técnica conhecida como cromatografia de afinidade de proteína A. O processo produz um alto fator de purificação - normalmente 99 por cento - mas é lento, criando assim um grande gargalo de produtividade. O processo é em grande parte dificultado pela baixa capacidade da proteína A, que se liga a anticorpos monoclonais a uma taxa média de 50 gramas por litro de meio de cromatografia de proteína A. O processo de purificação geral requer que anticorpos não purificados passem por colunas compactadas com a mídia em vários ciclos que podem levar até uma semana.
p Uma equipe de pesquisa liderada por Pete Gagnon e colegas de trabalho do A * STAR Bioprocessing Technology Institute em Cingapura desenvolveram um método alternativo com 1, 000 vezes a capacidade da proteína A. A técnica envolve o uso de polietilenoglicol, que faz com que os anticorpos sejam depositados na superfície das nanopartículas magnéticas revestidas com amido (ver imagem). As partículas são coletadas em um campo magnético, contaminantes não depositados são lavados e os anticorpos purificados são recuperados removendo o polietilenoglicol.
p "A alta capacidade do nosso método de nanopartículas o torna muito mais rápido do que a cromatografia em coluna, "explica Gagnon." Em vez da norma da indústria farmacêutica de cinco a oito ciclos, o novo processo requer apenas um ciclo, que leva apenas algumas horas. "Essa redução aumenta drasticamente a produtividade da nova abordagem em relação aos métodos tradicionais.
p O novo método também exigiu que a equipe de pesquisa desenvolvesse novas condições operacionais. O polietilenoglicol tem sido usado há décadas para processar anticorpos, mas nunca atingiu o nível de pureza necessário para a terapêutica clínica. A equipe descobriu que, ao elevar a concentração de sal, eles poderiam reduzir os níveis de contaminantes de cerca de 250, 000 partes por milhão a 500:o mesmo nível alcançado pela proteína A. Uma única etapa de polimento subsequente usando uma coluna de cromatografia multimodal purificou ainda mais os anticorpos de acordo com os padrões de qualidade clínica.
p Gagnon observa o alto potencial de adoção da nova tecnologia pela indústria. Além de resolver o problema de longa data de produtividade para anticorpos monoclonais, a abordagem de nanopartículas pode ser aplicada a muitas outras proteínas terapêuticas e também a vacinas virais.
