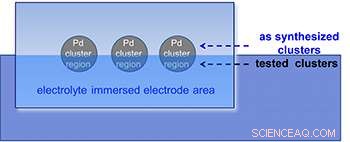
Um esquema do experimento de raios-X usado para determinar a estabilidade e composição do cluster (isto é, estado de oxidação).
(Phys.org) —O sonho de uma economia de hidrogênio - um mundo movido a H 2 gás, livre da poluição e da política dos combustíveis fósseis - pode depender do desenvolvimento de uma estratégia de eficiência energética para dividir a água em oxigênio e hidrogênio. O problema é que as ligações de água são muito estáveis, exigindo grandes entradas de energia para quebrar. Os cientistas estão desenvolvendo avidamente catalisadores para reduzir as demandas de energia, e, portanto, o custo, de H 2 Produção. Ainda, eles ainda lutam com o básico, tais como quais propriedades estruturais fazem um bom catalisador de divisão de água.
Usando medições da linha de luz 10-ID-B da equipe de pesquisa de materiais de acesso colaborativo (MR-CAT) e da Divisão de ciência de raios-X 12-ID-C, Linha de luz D na Fonte Avançada de Fótons (APS) do Departamento de Energia dos EUA, pesquisadores analisaram a estabilidade e a composição de três pequenos aglomerados de paládio - Pd 4 , Pd 6 , e Pd 17 - que estão sendo investigados como potenciais catalisadores de divisão da água. Eles então geraram modelos estruturais dos catalisadores. Ao combinar informações sobre a identidade e estrutura de cada cluster com sua atividade catalítica, os pesquisadores identificaram uma ligação Pd-Pd particular que parece ser essencial para a função catalítica. Esta pesquisa permitirá aos cientistas projetar melhores catalisadores de separação de água.
A divisão eletroquímica da água ocorre em duas reações distintas:a reação de evolução de hidrogênio (HER), e a reação de evolução de oxigênio (REA). Neste estudo, Os pesquisadores, do Laboratório Nacional de Argonne, a Universidade de Birmingham (Reino Unido), e a Universidade de Yale com foco em REA, que atualmente é a parte menos eficiente do processo de divisão da água. Estudos anteriores mostraram que o metal de platina pode catalisar REA, mas esses materiais requerem uma alta carga do metal caro, geralmente presente como grandes nanopartículas.
Em busca de um custo mais eficiente, mais eficiente em energia, e opções mais ativas, o estudo atual concentra-se em catalisadores de paládio com tamanhos inferiores a um nanômetro.
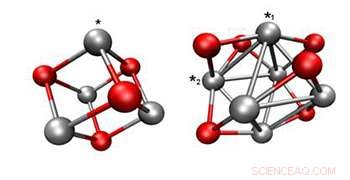
Possíveis estruturas de Pd 4 O 4 (esquerda) e Pd 6 O 6 (direita) gerado por cálculos funcionais de densidade.
Tipicamente, catalisadores metálicos são espalhados de forma um tanto aleatória nas superfícies de suporte, resultando em distribuições desconhecidas de átomos individuais, clusters, e partículas maiores. Para este estudo, os pesquisadores isolaram aglomerados de tamanhos específicos enviando um feixe molecular de íons de paládio através de um espectrômetro de massa, filtrando todos os tamanhos de partículas, exceto os aglomerados de interesse:Pd 4 , Pd 6 , e Pd 17 . Os clusters foram então imediatamente depositados, separadamente, em um eletrodo que consiste em uma pastilha de silício revestida com um filme fino de nanodiamante (primeira figura).
Para testar a capacidade catalítica dos pequenos aglomerados de paládio, os cátodos foram mergulhados, a meio caminho, em uma solução básica, que é o meio padrão usado em REA. Então, os pesquisadores realizaram voltametria, usando a corrente como uma medida da taxa de rotação da reação OER. A corrente gerada pelo cátodo contendo Pd 4 clusters não era melhor, e talvez um pouco pior, do que o eletrodo sozinho. Contudo, o Pd 6 e Pd 17 clusters mostraram atividade significativa, com taxas de rotatividade que superam as do trabalho anterior em superfícies de metal Pd e são comparáveis às do irídio, o catalisador de metal mais ativo para REA.
A próxima etapa foi caracterizar as amostras do cluster. Os pesquisadores trouxeram os mesmos eletrodos revestidos de cluster usados nos estudos de voltametria para o APS para caracterização por espectroscopia de absorção de raios-x de incidência rasante (GIXAS) na linha de luz 10-ID-B e espalhamento de raios-X de baixo ângulo de incidência rasante (GISAXS) em linha de luz 12-ID-C, D.
Uma observação importante foi que os aglomerados imersos parecem praticamente idênticos àqueles que não foram sujeitos à reação de oxidação da água, sugerindo que nem a catálise nem o ambiente básico hostil mudaram a estrutura dos aglomerados. Essa estabilidade é a chave para o desenvolvimento de catalisadores duráveis. Os estados de oxidação medidos do Pd 4 e Pd 6 os clusters foram usados em cálculos funcionais de densidade que determinaram, para cada cluster, as configurações estruturais (segunda figura), bem como a energia livre para cada etapa do REA.
Cálculos teóricos realizados usando o cluster de computação de alto desempenho no Centro de Materiais em Nanoescala da Argonne sugerem que os locais de Pd-Pd de ponte estão ativos para a reação de evolução de oxigênio (OER) em Pd 6 O 6 . Geral, um descritor chave para um catalisador OER Pd eficiente é um equilíbrio das diferenças de energia de ligação em relação à água líquida para cada um dos intermediários de reação importantes (O, OH, e OOH). Para esses clusters Pd, OOH é mais fortemente ligado do que as outras espécies, resultando no superpotencial observado. O pacote de teoria funcional da densidade VASP foi usado para obter essa visão sobre o mecanismo, e as estruturas de cluster foram obtidas usando o Algoritmo Genético de Cluster de Birmingham.
Os pesquisadores concluíram que a diferença pertinente entre os clusters era a presença de ligações Pd-Pd particulares nos dois clusters maiores, mas não no cluster menor. Eles suspeitam que esta ligação pode ser necessária para a catálise REA, sugerindo que as superfícies catalíticas podem ser impedidas por espécies inativas. A esperança é que, com o conhecimento do que constitui uma espécie ativa, os pesquisadores podem se concentrar em fazer catalisadores de divisão de água usando apenas os melhores clusters.