O aquecimento está ligado para baterias recarregáveis de óxido de manganês de sódio
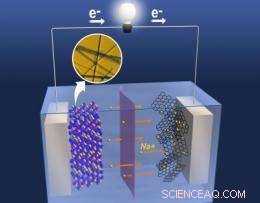 p A nanoestrutura uniforme de óxido de manganês tratado termicamente fornece túneis para os íons de sódio fluírem, melhorando o desempenho dos eletrodos. Crédito:PNNL
p A nanoestrutura uniforme de óxido de manganês tratado termicamente fornece túneis para os íons de sódio fluírem, melhorando o desempenho dos eletrodos. Crédito:PNNL
p (PhysOrg.com) - Ao adicionar a quantidade certa de calor, pesquisadores desenvolveram um método que melhora a capacidade elétrica e a vida útil de recarga de baterias recarregáveis de íon de sódio, o que poderia ser uma alternativa mais barata para usos em grande escala, como armazenamento de energia na rede elétrica. p Para conectar fontes de energia solar e eólica à rede elétrica, gerentes de rede requerem baterias que podem armazenar grandes quantidades de energia gerada na fonte. As baterias recarregáveis de íon de lítio - comuns em produtos eletrônicos de consumo e veículos elétricos - funcionam bem, mas são muito caros para uso generalizado na rede porque muitas baterias serão necessárias, e provavelmente precisarão ser grandes. O sódio é a segunda melhor escolha, mas as baterias de sódio-enxofre atualmente em uso funcionam a temperaturas acima de 300 graus Celsius, ou três vezes a temperatura da água fervente, tornando-os menos eficientes em termos de energia e seguros do que as baterias que funcionam em temperatura ambiente.
p Os desenvolvedores de baterias querem o melhor dos dois mundos - usar sódio barato e usar o tipo de eletrodo encontrado em recarregáveis de lítio. Uma equipe de cientistas do Laboratório Nacional do Noroeste do Pacífico do Departamento de Energia e pesquisadores visitantes da Universidade de Wuhan em Wuhan, A China usou nanomateriais para fazer eletrodos que podem trabalhar com sódio, eles relataram 3 de junho online no jornal
Materiais avançados .
p "A bateria de íon de sódio funciona em temperatura ambiente e usa íons de sódio, um ingrediente do sal de cozinha. Portanto, será muito mais barato e seguro, "disse o químico do PNNL Jun Liu, que co-liderou o estudo com o químico Yuliang Cao da Universidade de Wuhan.
p Os eletrodos recarregáveis de lítio que interessam aos pesquisadores são feitos de óxido de manganês. Os átomos neste óxido metálico formam muitos buracos e túneis pelos quais os íons de lítio viajam quando as baterias estão sendo carregadas ou em uso. O movimento livre dos íons de lítio permite que a bateria retenha eletricidade ou libere-a em uma corrente. Mas simplesmente substituir os íons de lítio por íons de sódio é problemático - os íons de sódio são 70% maiores do que os íons de lítio e não cabem nas fendas também.
p Para encontrar uma maneira de fazer buracos maiores no óxido de manganês, Os pesquisadores do PNNL ficaram muito menores. Eles se voltaram para nanomateriais - materiais feitos em escala nanométrica, ou cerca de um milhão de vezes mais fino do que uma moeda - que têm propriedades surpreendentes devido à sua pequenez. Por exemplo, as curtas distâncias que os íons de sódio têm que percorrer em nanofios podem tornar o óxido de manganês um eletrodo melhor de maneiras não relacionadas ao tamanho dos túneis.
p Explorar, a equipe misturou dois tipos diferentes de blocos de construção atômicos de óxido de manganês - um cujos átomos se organizam em pirâmides, e outro cujos átomos formam um octaedro, uma estrutura semelhante a um diamante de duas pirâmides unidas em suas bases. Eles esperavam que o material final tivesse grandes túneis em forma de S e túneis menores de cinco lados através dos quais os íons pudessem fluir.
p Depois de misturar, a equipe tratou os materiais com temperaturas variando de 450 a 900 graus Celsius, em seguida, examinou os materiais e testou qual tratamento funcionou melhor. Usando um microscópio eletrônico de varredura, a equipe descobriu que temperaturas diferentes criavam material de qualidade diferente. O tratamento do óxido de manganês a 750 graus Celsius criou os melhores cristais:muito baixos e os cristais pareciam flácidos, muito alto e os cristais se transformaram em placas planas maiores.
p Ampliando ainda mais usando um microscópio eletrônico de transmissão na EMSL, Laboratório de Ciências Moleculares Ambientais do DOE no campus do PNNL, a equipe viu que o óxido de manganês aquecido a 600 graus tinha marcas nos nanofios que poderiam impedir os íons de sódio, mas os fios tratados com 750 graus pareciam uniformes e muito cristalinos.
p Mas mesmo o material mais bonito é apenas uma fachada, se não funcionar bem. Para descobrir se ele correspondia à sua boa aparência, a equipe PNNL-Wuhan mergulhou o material do eletrodo em eletrólito, o líquido contendo íons de sódio que ajudará os eletrodos de óxido de manganês a formar uma corrente. Em seguida, eles carregaram e descarregaram as células da bateria experimental repetidamente.
p A equipe mediu a capacidade de pico em 128 miliampères horas por grama de material do eletrodo conforme a célula da bateria experimental descarregava. Este resultado superou os anteriores obtidos por outros pesquisadores, um dos quais atingiu a capacidade máxima de 80 miliamperes hora por grama para eletrodos feitos de óxido de manganês, mas com um método de produção diferente. Os pesquisadores acreditam que a capacidade mais baixa se deve aos íons de sódio que causam mudanças estruturais naquele óxido de manganês que não ocorrem ou ocorrem com menos frequência no material nanométrico tratado termicamente.
p Além de alta capacidade, o material resistiu bem aos ciclos de carga e descarga, como ocorreria no uso do consumidor. Novamente, o material tratado a 750 Celsius teve o melhor desempenho:após 100 ciclos de carga e descarga, ele perdeu apenas 7% de sua capacidade. O material tratado a 600 Celsius ou 900 Celsius perdeu cerca de 37 por cento e 25 por cento, respectivamente.
p Mesmo depois de 1, 000 ciclos, a capacidade dos eletrodos tratados com 750 Celsius caiu apenas cerca de 23 por cento. Os pesquisadores acharam que o material funcionou muito bem, retendo 77 por cento de sua capacidade inicial.
p Último, a equipe carregou a célula experimental em velocidades diferentes para determinar a rapidez com que poderia consumir eletricidade. A equipe descobriu que quanto mais rápido eles carregavam, menos eletricidade poderia conter. Isso sugeriu à equipe que a velocidade com que os íons de sódio podiam se difundir no óxido de manganês limitava a capacidade da célula da bateria - quando carregada rapidamente, os íons de sódio não podiam entrar nos túneis rápido o suficiente para enchê-los.
p Para compensar os lentos íons de sódio, os pesquisadores sugerem que no futuro eles façam nanofios ainda menores para acelerar o carregamento e a descarga. As baterias da rede precisam de carregamento rápido para que possam coletar o máximo possível de energia recém-produzida proveniente de fontes renováveis. E eles precisam descarregar rapidamente quando a demanda aumenta, à medida que os consumidores ligam seus aparelhos de ar-condicionado e televisão, e conecte seus veículos elétricos em casa.
p Essas baterias de alto desempenho poderiam tirar o calor de uma rede de energia elétrica já sobrecarregada.
