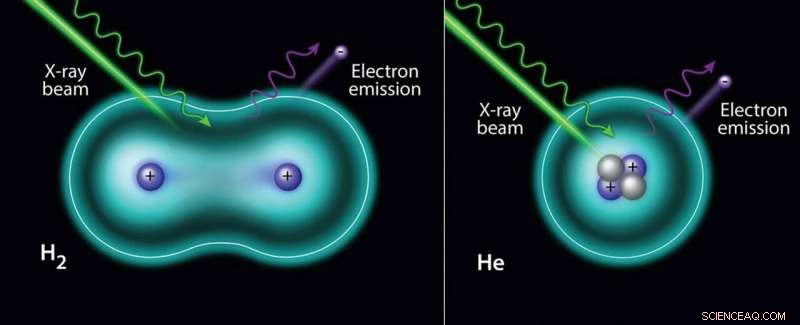
O feixe de raios X induz a foto-ejeção de um elétron do hidrogênio (esquerdo) e do hélio (direito). Crédito:Departamento de Energia dos EUA
Pela primeira vez, os cientistas mediram a estrutura vibracional dos átomos de hidrogênio e hélio por meio de raios-X. Os resultados refutam o equívoco de que é impossível obter espectros de espectroscopia de fotoelétrons de raios-X (XPS) de hidrogênio e hélio, os dois elementos mais leves da Tabela Periódica. Acredita-se que esse seja o caso devido às baixas probabilidades de ejeção de elétrons desses elementos induzida por raios-X.
O brilho incomparável do feixe na National Synchrotron Light Source-II aumenta significativamente a probabilidade de um fóton colidir com um átomo de gás à pressão ambiente. A linha de luz torna possível usar o XPS para estudar diretamente os dois elementos mais abundantes do universo.
Também, este trabalho ajuda a descrever os limites do XPS, abrindo um escopo mais amplo para uma das técnicas mais úteis na ciência dos materiais.
A espectroscopia de fotoelétrons de raios X (XPS) é uma das técnicas mais poderosas da ciência dos materiais. Contudo, a literatura está repleta de afirmações afirmando que é impossível usar o XPS para estudar os dois elementos mais leves e abundantes do universo, hidrogênio e hélio.
Este trabalho demonstrou que os espectros de fotoelétrons de raios-X de hidrogênio e hélio à pressão ambiente podem ser obtidos quando uma fonte de raios-X brilhante é usada, como no National Synchrotron Light Source II.
No caso do gás hélio, o espectro mostra um pico simétrico de seu único orbital. No caso de moléculas de gás hidrogênio, um pico assimétrico é observado, que está relacionado aos diferentes modos vibracionais possíveis do estado final. A estrutura vibracional da molécula de hidrogênio é evidente no H 2 Espectro de 1s.