Os pesquisadores criam organelas artificiais para controlar o comportamento celular
 p Proteínas intrinsecamente desordenadas (verde fluorescente) aglomeram-se dentro das células para formar organelas artificiais. Crédito:Duke University
p Proteínas intrinsecamente desordenadas (verde fluorescente) aglomeram-se dentro das células para formar organelas artificiais. Crédito:Duke University
p Os engenheiros biomédicos da Duke University demonstraram um método para controlar a separação de fases de uma classe emergente de proteínas para criar organelas artificiais sem membrana dentro das células humanas. O avanço, semelhante a controlar como o vinagre forma gotículas dentro do óleo, cria oportunidades para a engenharia de estruturas sintéticas para modular funções celulares existentes ou criar comportamentos inteiramente novos dentro das células. p Os resultados aparecem online no dia 3 de agosto na revista
Química da Natureza .
p As proteínas funcionam dobrando-se em formas 3-D específicas que interagem com diferentes estruturas biomoleculares. Os pesquisadores acreditavam que as proteínas precisavam dessas formas fixas para funcionar. Mas nas últimas duas décadas, uma grande nova classe de proteínas intrinsecamente desordenadas (IDPs) foram descobertas que têm grandes regiões que são "flexíveis" - isto é, eles não se dobram em uma forma 3-D definida. Agora entende-se que essas regiões desempenham um importante, papel anteriormente não reconhecido no controle de várias funções celulares.
p Os IDPs também são úteis para aplicações biomédicas porque podem sofrer transições de fase - mudando de um líquido para um gel, por exemplo, ou de um estado solúvel para um insolúvel, e vice-versa - em resposta a gatilhos ambientais, como mudanças de temperatura. Essas características também ditam seu comportamento de fase em ambientes celulares e são controladas pelo ajuste de características dos IDPs, como seu peso molecular ou a sequência na qual os aminoácidos estão ligados.
p "Embora existam muitos IDPs naturais que mostram comportamento de fase nas células, eles vêm em muitos sabores diferentes, e tem sido difícil discernir as regras que governam esse comportamento, "disse Ashutosh Chilkoti, o Distinto Professor Alan L. Kaganov de Engenharia Biomédica na Duke. "Este artigo fornece princípios de engenharia muito simples para programar esse comportamento dentro de uma célula."
p "Outros no campo adotaram uma abordagem de cima para baixo, onde farão uma mudança em um IDP natural e verão como seu comportamento muda dentro de uma célula, "disse Michael Dzuricky, um cientista pesquisador que trabalha no laboratório de Chilkoti e primeiro autor do estudo. "Estamos adotando a abordagem oposta e construindo nossos próprios PDIs artificiais a partir de princípios termodinâmicos simples. Isso permite que nós e outros sintonizemos com precisão uma única propriedade - a forma do diagrama de fases dos PDIs - para entender melhor como esse parâmetro afeta o comportamento biológico"
p No novo jornal, os pesquisadores começam procurando na natureza exemplos de IDPs que se juntam para formar "condensados biomoleculares" dentro das células. Essas estruturas fracamente mantidas juntas permitem que as células criem compartimentos sem também construir uma membrana para encapsulá-los. Usando um PDI da mosca da fruta comum como base, os pesquisadores extraem de sua extensa história de trabalho com IDPs para criar uma versão artificial molecularmente mais simples que mantém o mesmo comportamento.
p Esta versão mais simples permitiu aos pesquisadores fazer alterações precisas no peso molecular do IDP e nos aminoácidos dos IDPs. Os pesquisadores mostram que, dependendo de como essas duas variáveis são ajustadas, os IDPs se reúnem para formar esses compartimentos em diferentes temperaturas em um tubo de ensaio. E ao tentar consistentemente vários ajustes e temperaturas, os pesquisadores obtiveram uma compreensão sólida de quais parâmetros de projeto são mais importantes para controlar o comportamento do IDP.
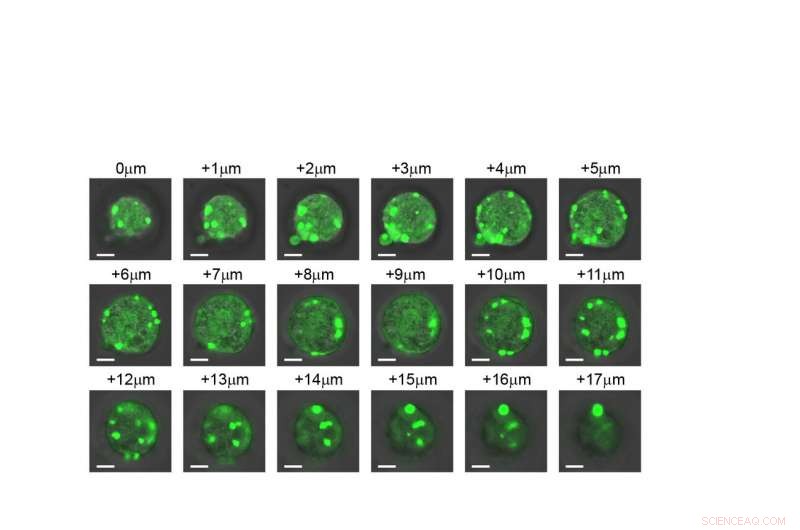 p Uma visão fatia a fatia de uma célula, mostrando que as organelas artificiais se formam em toda a estrutura. Crédito:Duke University
p Uma visão fatia a fatia de uma célula, mostrando que as organelas artificiais se formam em toda a estrutura. Crédito:Duke University
p Um tubo de ensaio, Contudo, não é o mesmo que uma célula viva, então os pesquisadores deram um passo adiante para demonstrar como seus IDPs projetados se comportam dentro da E. coli. Como previsto, seus IDPs artificiais se agruparam para formar uma pequena gota dentro do citoplasma da célula. E porque o comportamento do IDP era agora tão bem compreendido, os pesquisadores mostraram que podiam controlar de forma previsível como eles se aglutinavam usando seus princípios de tubo de ensaio como um guia.
p "Fomos capazes de alterar as temperaturas nas células para desenvolver uma descrição completa de seu comportamento de fase, que espelhou nossas previsões de tubo de ensaio, "disse Dzuricky." Neste ponto, fomos capazes de projetar diferentes sistemas IDP artificiais, onde as gotículas formadas têm diferentes propriedades materiais. "
p Dito de outra forma, porque os pesquisadores entenderam como manipular o tamanho e a composição dos IDPs para responder à temperatura, eles poderiam programar os IDPs para formar gotículas ou compartimentos de densidades variadas dentro das células. Para mostrar como essa capacidade pode ser útil para engenheiros biomédicos, os pesquisadores então usaram seus novos conhecimentos, como a natureza costuma fazer, para criar uma organela que desempenha uma função específica dentro de uma célula.
p Os pesquisadores mostraram que poderiam usar os IDPs para encapsular uma enzima para controlar seu nível de atividade. Ao variar o peso molecular dos IDPs, os IDPs retêm a enzima tanto aumentada quanto diminuída, o que por sua vez afetou o quanto ele poderia interagir com o resto da célula.
p Para demonstrar essa habilidade, os pesquisadores escolheram uma enzima usada pela E. coli para converter lactose em açúcares utilizáveis. Contudo, nesse caso, os pesquisadores rastrearam a atividade desta enzima com um repórter fluorescente em tempo real para determinar como a organela IDP projetada estava afetando a atividade da enzima.
p No futuro, os pesquisadores acreditam que poderiam usar suas novas organelas IDP para controlar os níveis de atividade de biomoléculas importantes para os estados de doença. Ou para aprender como os deslocados internos naturais desempenham funções celulares semelhantes e entender como e por que às vezes funcionam mal.
p "Esta é a primeira vez que alguém consegue definir com precisão como a sequência da proteína controla o comportamento de separação de fases dentro das células, "disse Dzuricky." Usamos um sistema artificial, mas achamos que as mesmas regras se aplicam aos deslocados internos naturais e estamos ansiosos para começar a testar essa teoria. "
p "Também podemos começar a programar esse tipo de comportamento de fase com qualquer proteína em uma célula, fundindo-as a esses IDPs artificiais, "disse Chilkoti." Esperamos que esses deslocados artificiais forneçam uma nova ferramenta para a biologia sintética controlar o comportamento das células.

