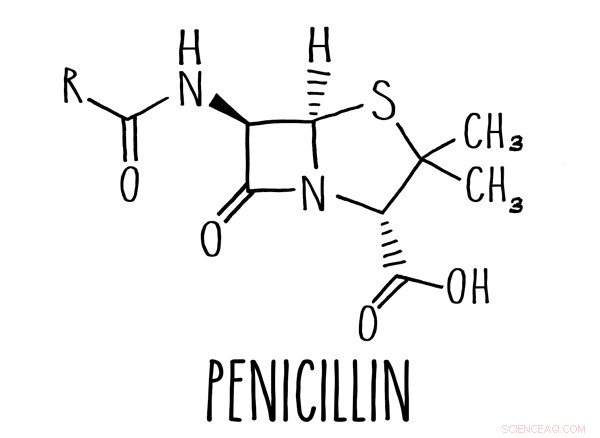
Um anel beta-lactâmico é a base de muitos antibióticos, incluindo penicilina. Crédito:Caltech
Na corrida armamentista em curso com humanos e seus antibióticos de um lado, e bactérias com sua capacidade de desenvolver defesas para antibióticos, por outro lado, os humanos alistaram um novo aliado - outras bactérias.
Muitos antibióticos comuns, incluindo o antibiótico mais famoso, penicilina, baseiam-se em uma estrutura molecular conhecida como anel beta-lactama. Essas drogas, apropriadamente chamados de antibióticos beta-lactâmicos, interfere na capacidade da bactéria de construir sua parede celular.
À medida que as bactérias desenvolvem resistência aos antibióticos existentes, pesquisadores e empresas farmacêuticas trabalham para criar novos. Isso significa que muito trabalho é feito para criar novos tipos de beta-lactâmicos, e é aí que o laboratório de Frances Arnold entra em cena.
Os beta-lactâmicos são feitos pegando uma molécula em forma de cadeia e enrolando-a, É como pegar uma ponta de um barbante e dar um nó no meio do barbante.
O principal desafio é controlar precisamente onde ao longo da molécula a reação ocorre. Com a química sintética tradicional, os químicos precisam pregar peças extras nas moléculas que desejam transformar em beta-lactâmicos. Sem essas peças extras, os nós vão acabar amarrados em pontos inconsistentes, resultando em alguns loops grandes e outros pequenos. Isso é indesejável para quem está tentando fabricar um lote consistente de antibióticos. Mas a adição dessas peças extras torna a síntese mais complicada porque etapas adicionais são necessárias para adicioná-las e ainda mais etapas para removê-las após a conclusão do loop.

Um anel lactama é criado enrolando uma molécula sobre si mesma, muito parecido com amarrar um laço em um pedaço de corda. Crédito:Caltech
A estudante de graduação Inha Cho e a bolsista de pós-doutorado Zhi-Jun Jia, ambos do laboratório de Arnold, desenvolveram algo mais simples usando a evolução direcionada, uma técnica desenvolvida por Arnold, o Professor Linus Pauling de Engenharia Química, Bioengenharia e Bioquímica, e diretor do Donna e Benjamin M. Rosen Bioengineering Center. Na evolução dirigida, que Arnold desenvolveu na década de 1990 e pelo qual recebeu o Prêmio Nobel de Química de 2018, as enzimas são desenvolvidas em um laboratório até que se comportem da maneira desejada. O código genético de uma enzima útil é transferido para bactérias como a Escherichia coli. À medida que as bactérias crescem, dividir, e continuar suas vidas, eles produzem a enzima.
Nesse caso, Cho e Jia tomaram uma enzima conhecida como citocromo P450, que tem sido um burro de carga versátil no laboratório de Arnold, e evoluiu para produzir beta-lactâmicos. Duas outras versões de enzimas também foram criadas para construir outros tamanhos de anel de lactamas. Uma versão cria uma gama-lactama, um ciclo de quatro átomos de carbono e um átomo de nitrogênio. E a outra versão cria um delta-lactama, um ciclo de cinco átomos de carbono e um átomo de nitrogênio.
“Estamos desenvolvendo novas enzimas com atividades que não podem ser encontradas na natureza, "diz Cho." Os lactâmicos podem ser encontrados em muitos medicamentos diferentes, mas especialmente em antibióticos, e estamos sempre precisando de novos. "
Jia ressalta que as enzimas que eles criaram também são incrivelmente eficientes, com cada molécula de enzima capaz de produzir até um milhão de moléculas de beta-lactama. "Eles representam as enzimas mais eficientes criadas em nosso laboratório, e estão prontos para aplicações industriais, "Jia diz.
O papel, intitulado "Amidação C-H enzimática local-seletiva para a síntese de diversas lactamas" e co-autoria de Arnold, aparece na edição de 10 de maio de Ciência .