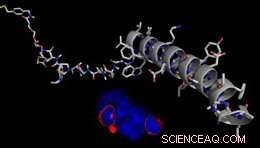
Modelo de um AgONista Clivável REdutivamente (RECON) para o controle reversível de vias de sinalização celular dependentes de GPCR. Crédito:J. Broichhagen, D. Hodson
Os pesquisadores do LMU desenvolveram um método que permite que os receptores da superfície celular sejam ligados e desligados à vontade. A técnica promete fornecer novos insights sobre as funções do receptor e seus efeitos nas vias de sinalização intracelular.
Os receptores transmembrana acoplados à proteína G (GPCRs) estão intimamente envolvidos na regulação de uma ampla gama de processos biológicos. Eles atuam ligando-se a moléculas mensageiras extracelulares - como hormônios - e ativando retransmissores de sinalização intracelular que alteram as funções celulares de maneiras específicas. Não surpreendentemente, defeitos funcionais nesses receptores ligados à membrana freqüentemente levam a distúrbios fisiológicos crônicos. Isso explica por que uma grande proporção da pesquisa farmacológica atual concentra-se em encontrar drogas que têm como alvo GPCRs específicos. Uma colaboração de pesquisa envolvendo grupos liderados pelos professores Anja Hoffmann-Röder (Professora de Química Orgânica) na LMU, Dirk Trauner (anteriormente LMU, agora na New York University) e David Hodson (University of Birmingham) já projetou um conjunto de moléculas com as quais GPCRs (e potencialmente outros tipos de receptores) podem ser farmacologicamente ativados e desativados à vontade. Esses agentes prometem descobrir novos aspectos dos mecanismos moleculares que fundamentam as ações dos receptores, e, ao fazê-lo, deve facilitar o desenvolvimento de novas estratégias terapêuticas. As novas descobertas aparecem no jornal online ACS Central Science .
O novo estudo é baseado em um trabalho anterior no qual a equipe desenvolveu um sistema farmacológico dependente de luz com o auxílio de 'tags SNAP'. Um SNAP-tag é uma proteína de ligação que pode ser introduzida em uma proteína receptora alvo por meios genéticos. Seu objetivo é atuar como um sítio de ligação para a fixação de um ligante sintético, que então pode modular a sinalização do receptor, ou seja, ativar ou bloquear a ativação. O novo artigo descreve a aplicação desta técnica a um receptor denominado GLP-1R, que regula a secreção de insulina. Portanto, apresenta um alvo atraente para o desenvolvimento de medicamentos para o tratamento do diabetes. "Usamos como ligante um hormônio natural equipado com uma extensão sintética que atua como um adaptador covalentemente ligado pelo SNAP-tag. A ligação do hormônio ativa o receptor, enquanto a conexão direta do adaptador à etiqueta SNAP garante que o receptor seja mantido no estado LIGADO, "explica Tom Podewin (Instituto Max Planck de Pesquisa Médica), co-primeiro autor do novo estudo e até 2017 doutorando no grupo de Hoffmann-Röder. A anexação da extremidade do adaptador à etiqueta SNAP efetivamente amarra o ligante ao receptor. Contudo, o adaptador é conectado de forma flexível ao local de ligação do hormônio do receptor por meio de uma ligação dissulfeto, que pode ser facilmente quebrado pela adição de um agente redutor. Este truque permite que o hormônio seja liberado de seu local de ligação, revertendo assim a interação e desligando o receptor novamente.
A fim de demonstrar a versatilidade desta abordagem de 'farmacologia tethered', a equipe usou um ligante sintético diferente para ativar um receptor que controla a secreção do hormônio do crescimento. "Nossos ligantes são, na verdade, as maiores moléculas presas conhecidas que atuam como ativadores ou agonistas dos receptores ligados à membrana. Isso prova que a farmacologia presa não se restringe ao uso de moléculas pequenas, mas pode ser estendido a peptídeos e talvez até mesmo a proteínas, "Hoffmann-Röder ressalta.
Uma vez que a ligação à etiqueta SNAP é covalente, o ligando de ativação não pode ser prontamente liberado do receptor na ausência de um agente redutor. Normalmente, os GPCRs ativados são imediatamente removidos da membrana celular e transportados para as vesículas intracelulares. Uma vez lá, seus ligantes se dissociam e são então reciclados para a superfície da célula. Contudo, os pesquisadores descobriram - para sua surpresa - que a ligação do ligante sintético inibe esse processo de reciclagem, aprisionando o receptor na vesícula. "A capacidade de anexar de forma duradoura qualquer ligante - seja um agente farmacológico ou uma etiqueta para uso em bioimagem - a um receptor adequadamente modificado oferece novas oportunidades para a manipulação e caracterização de vias de sinalização complexas nas células, "acrescenta o primeiro autor em conjunto, Johannes Broichhagen. Ele e seus colegas acreditam que o novo método trará uma melhor compreensão dos receptores e suas funções, o que sem dúvida terá repercussões no desenvolvimento de medicamentos no futuro.