
A água é diferente de outras substâncias porque sua forma sólida - como este iceberg - é menos densa que sua forma líquida - como este oceano. Os cientistas estão estudando outras propriedades estranhas da água. Crédito:Wikimedia Commons
A água tem muitas propriedades incomuns, como sua forma sólida, gelo, ser capaz de flutuar em água líquida, e eles ficam mais estranhos abaixo de seu ponto de congelamento. Água super-resfriada - abaixo de zero, mas ainda líquida - é notoriamente difícil de estudar. Alguns pesquisadores pensaram que a água super-resfriada se comportou de forma estranha dentro de uma faixa particularmente fria, passando de um líquido para um sólido, cristalizando instantaneamente em uma determinada temperatura, como algo saído de um romance de Kurt Vonnegut.
Agora, pesquisadores descobriram uma maneira de tirar fotos da água congelando dentro dessa faixa super-resfriada. E adivinha? A água não é tão estranha quanto poderia ser. A água líquida pode existir em todo o caminho, cristalizando em um sólido mais lentamente conforme as coisas ficam mais frias, como esperado, mas nunca de uma vez.
Uma equipe de pesquisadores do Laboratório Nacional do Noroeste do Pacífico do Departamento de Energia relatou o trabalho no Proceedings of the National Academy of Sciences Edição antecipada online. Embora os resultados não mudem a maneira como você faz seu chá gelado no verão, pode ajudar os teóricos a aprofundar sua compreensão da água e ajudar os cientistas atmosféricos a entender melhor a chuva e as nuvens.
Um truque estranho de água
A maioria das pessoas sabe que o gelo flutua na água líquida, mas eles podem não estar cientes de que a água tem dificuldade em formar um copo. Um vidro - como uma janela - é um sólido no qual as moléculas estão realmente organizadas como estariam em um líquido.
Pegue um monte de laranjas. Laranjas amontoadas livremente em um saco são como um líquido - as moléculas individuais podem se mover livremente. Se você embalar as laranjas ordenadamente em uma caixa, você forma um cristal. Se você apertar o saco e impedir que as laranjas misturadas se movam, mas sem organizá-las corretamente, você forma um copo.
Óculos são ótimos porque podem conter contaminantes - pense em uma mosca no âmbar, ou lixo nuclear em vidro vitrificado - enquanto os cristais expelem contaminantes - congelar a água do mar é uma forma de dessalinizá-la. Para fazer um copo, pesquisadores derretem areia ou outro componente até que se torne líquido. E então eles esfriam tão rápido que não pode formar um cristal antes de solidificar.
Mas congele a água a granel rapidamente e ela não formará um copo. Rapidamente se transforma em gelo. Para se tornar vidro, a água líquida deve ser resfriada a uma temperatura profundamente abaixo de zero em microssegundos - cerca de 136 Kelvin (cerca de 215 graus F negativos), uma temperatura comum no espaço sideral, onde alguns esperam que exista água vítrea.
A faixa que tem sido difícil de estudar está ligeiramente acima da chamada temperatura de transição vítrea. Os cientistas não sabem o que está acontecendo entre cerca de 160 e 235 K. (Na vida real, que fica entre a temperatura na lua de Marte, Fobos e Fairbanks, Alasca, nas profundezas do inverno.) Na extremidade superior dessa faixa (perto de 235 K, Fairbanks), água congela de um líquido super-resfriado a um cristal em milissegundos, o que é muito rápido para as técnicas analíticas atuais estudarem.
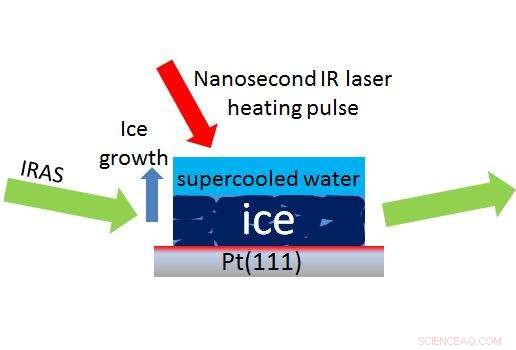
Um laser (seta vermelha) cria uma pequena gota de água super-resfriada sobre o gelo, permitindo que os cientistas usem um método chamado IRAS (setas verdes) para medir em nanossegundos a velocidade com que a água super-resfriada se transforma em gelo. Crédito:Kay, Kimmel / PNNL
Os cientistas tiveram uma variedade de ideias para explicar o que pode estar acontecendo naquela região inexplorada. Eles se perguntaram se a água permaneceria metaestável - líquida, mas pronta para começar a cristalizar a qualquer momento - até a temperatura em que se torna um vidro. Ou se o líquido se tornasse instável em algum lugar mais quente do que isso, por volta de 228 K (um pouco mais quente do que o recorde da estação McMurdo na Antártica), nesse ponto, ele se cristalizaria espontaneamente devido ao que os físicos chamam de singularidade. Também, algo dentro desse intervalo pode estar acontecendo que pode ajudar a explicar por que a água tem dificuldade em formar um copo.
"Havia uma infinidade de postulados, mas uma escassez de dados, "disse o físico químico da PNNL, Bruce Kay.
"Nosso objetivo era desenvolver uma nova técnica para aquecer e resfriar rapidamente filmes de água super-resfriados em nanoescala, "disse o físico do PNNL Greg Kimmel.
O mistério dentro
Para obter os dados nesse intervalo incomensurável, Kimmel e Kay trabalharam com Yuntao Xu, um especialista em laser, e outros na PNNL e desenvolveram uma maneira de aquecer e resfriar água em escalas de tempo de nanossegundos com um laser. Usando este método, os cientistas do PNNL mediram a rapidez com que a água super-resfriada se converteu em gelo cristalino à medida que a temperatura diminuía. O tempo de cristalização caiu de nanossegundos perto das temperaturas mais altas para horas a 126 K. Em nenhum momento, especialmente a 228 K, a água super-resfriada se transformou em um cristal, excluindo a possibilidade de uma singularidade.
Para procurar a singularidade de outro ângulo, os pesquisadores exploraram o quão rápido as moléculas de água super-resfriada podem se mover, e o quanto isso mudou conforme ficou mais frio. Se a singularidade existisse, eles esperariam que as moléculas de água fossem incapazes de se mover em algum ponto. Do ponto de congelamento até o ponto de vidro, as moléculas se moviam cada vez mais devagar de maneira complexa, mas contínua. Geral, a relação entre a temperatura e a rapidez com que as moléculas se moviam não sugeria uma singularidade a 228 K.
"Provavelmente podemos tirar a singularidade da mesa, "disse Kay do PNNL.
Tomados em conjunto, os resultados fornecem informações valiosas sobre como a água se comporta.
"Por exemplo, na química atmosférica, gotas de água super-resfriadas são encontradas nas nuvens. Existem dúvidas sobre por quanto tempo eles persistem, "disse Kimmel do PNNL.