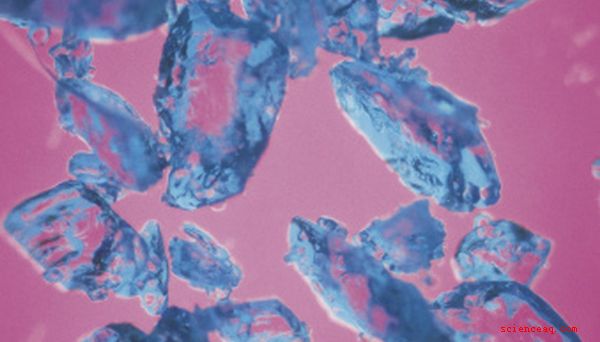
Como muitos complexos de metais de transição, o sulfato de cobre (II) penta-hidratado é colorido; cristais desta substância bonita são um tom pálido de azul. Sua cor deriva da química e da física de sua composição - ou, mais especificamente, do tipo de ligação que se forma com os íons sulfato e as moléculas de água ligadas ao cobre.
Orbitais
Os elétrons exibem ondas dualidade de partículas, o que significa que elas têm propriedades semelhantes a ondas e propriedades semelhantes a partículas. O comportamento de um elétron em um átomo é descrito por uma equação semelhante a uma onda chamada função de onda. O quadrado da função de onda dá a probabilidade de que o elétron seja encontrado em qualquer ponto em particular e em um dado momento. As funções de onda dos elétrons nos átomos também são chamadas de orbitais atômicos. Os químicos nomeiam orbitais atômicos usando um número para designar o nível de energia do orbital seguido de uma letra para designar o tipo de orbital. Para elementos no quarto período da tabela periódica ou acima, você só precisa se concentrar em três tipos de orbitais, a saber, s, p e d. Para ter uma idéia do formato desses orbitais, consulte o link na seção de recursos.
Divisão de campos de cristal
O íon de cobre no sulfato de cobre (II) perdeu dois elétrons, portanto, possui um + 2 carga. Possui nove elétrons em seu nível de energia mais externo ou casca; todos os chamados elétrons de valência ocupam orbitais 3d. As moléculas de água e os íons sulfato são atraídos pela carga positiva do íon cobre, de modo que eles se aproximam e se organizam em uma configuração octaédrica. Consequentemente, dois dos cinco orbitais 3d do íon de cobre se alinham ao longo dos eixos pelos quais os íons sulfato e as moléculas de água se aproximam; como os elétrons nesses orbitais e os elétrons nas moléculas /íons têm carga negativa, eles se repelem. Por fim, dois dos cinco orbitais 3d aumentaram a energia; estes são chamados de orbitais eg. Os outros três, por outro lado, têm energia reduzida e são chamados orbitais t2g.
Absorção de luz
Um fóton de luz será absorvido pelo complexo de coordenação se tiver uma energia equivalente à diferença entre o estado que um elétron ocupa agora e a energia de outro estado à sua disposição. Consequentemente, o complexo de sulfato de cobre pode absorver fótons de luz com energias equivalentes à diferença de energia entre t2g e, por exemplo, orbitais. Por acaso, a diferença de energia para o complexo de sulfato de cobre é equivalente à diferença de energia para fótons de luz na região vermelho-laranja do espectro. Como a luz avermelhada é absorvida enquanto a luz azul é transmitida, o sulfato de cobre aparece azul.
Dissolvendo-se em Água
Quando o sulfato de cobre se dissolve na água, os íons cobre e sulfato se dissociam. Agora, o íon de cobre forma um complexo octaédrico, onde é cercado por seis moléculas de água. O efeito ainda é praticamente o mesmo, no entanto, porque a divisão entre orbitais t2g e, por exemplo, orbitais neste novo complexo ainda é tal que a luz laranja avermelhada é absorvida e você vê uma solução de cor azul.