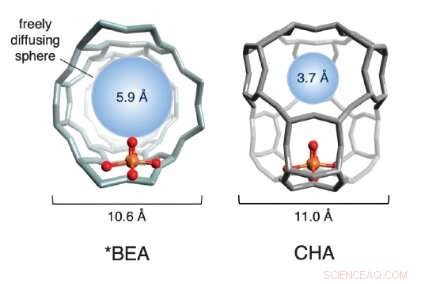
Uma ilustração das estruturas de gaiola de duas zeólitas à base de ferro usadas no estudo. As esferas vermelha e dourada (representando oxigênio e ferro, respectivamente) compõem o site ativo. A estrutura da gaiola, em cinza, isformado de silício, alumínio e oxigênio. A esfera azul quantifica o tamanho da maior molécula que pode se difundir livremente para dentro e para fora da gaiola do local ativo (o diâmetro do metano é ~ 4,2 Å). Crédito:Benjamin Snyder
Uma equipe de pesquisadores da Universidade de Stanford e da Universidade de Leuven, na Bélgica, elucidou ainda mais um processo intrigante que pode ser um passo importante em direção a uma economia de combustível de metanol com metano abundante como matéria-prima, um avanço que pode mudar fundamentalmente a forma como o mundo usa o gás natural.
Metanol - o álcool mais simples - é usado para fazer vários produtos, como tintas e plásticos, e como aditivo à gasolina. Rico em hidrogênio, o metanol pode impulsionar as células de combustível da nova era que podem gerar benefícios ambientais significativos.
Se o gás natural, do qual o metano é o principal componente, poderia ser convertido economicamente em metanol, o combustível líquido resultante seria armazenado e transportado com muito mais facilidade do que o gás natural e o hidrogênio puro. Isso também reduziria muito as emissões de metano das usinas de processamento de gás natural e dutos. Hoje, metano escapou, um gás de efeito estufa muitas vezes mais potente do que o dióxido de carbono, quase nega as vantagens ambientais do gás natural sobre o petróleo e o carvão. O novo estudo da equipe na edição atual do Ciência é o último deles a desenvolver uma forma de baixo consumo de energia para produzir metanol a partir do metano.
"Este processo usa cristais comuns conhecidos como zeólitas de ferro, que são conhecidos por converter gás natural em metanol em temperatura ambiente, "explica Benjamin Snyder, que obteve seu doutorado em Stanford estudando catalisadores para abordar as principais facetas desse desafio. "Mas, isso é uma química extremamente desafiadora de se alcançar em um nível prático, já que o metano é teimosamente inerte quimicamente. "
Quando o metano é infundido em zeólitas de ferro poroso, o metanol é rapidamente produzido à temperatura ambiente, sem necessidade de calor ou energia adicional. Por comparação, o processo industrial convencional para fazer metanol a partir do metano requer temperaturas de 1000 ° C (1832 ° F) e extrema alta pressão.
"Esse é um processo economicamente tentador, mas não é tão fácil. Barreiras significativas impedem o escalonamento deste processo para níveis industriais, "disse Edward Solomon, Professor de química e ciência de fótons de Stanford no SLAC National Accelerator Laboratory. Solomon é o autor sênior do novo estudo.
Mantendo as zeólitas ligadas
Infelizmente, a maioria das zeólitas de ferro se desativa rapidamente. Incapaz de processar mais metano, o processo se esgota. Os cientistas estão interessados em estudar maneiras de melhorar o desempenho do zeólito de ferro. O novo estudo, co-autoria de Hannah Rhoda, candidato a doutorado em Stanford em química inorgânica, usa espectroscopia avançada para explorar a estrutura física dos zeólitos mais promissores para a produção de metano em metanol.

Hannah Rhoda com o equipamento de espectroscopia Raman de ressonância, que dispara um laser em uma amostra para obter informações vibracionais do local exato que está sendo estudado. Os pesquisadores no estudo atual usaram essa técnica para ajudar a atribuir os locais envenenados por Fe (III) -OH e Fe (III) OCH3, que iluminou o mecanismo. Crédito:Hannah Rhoda
"Uma questão chave aqui é como retirar o metanol sem destruir o catalisador, "Disse Rhoda.
Escolhendo duas atraentes zeólitas de ferro, a equipe estudou a estrutura física das grades em torno do ferro. Eles descobriram que a reatividade varia dramaticamente de acordo com o tamanho dos poros na estrutura cristalina circundante. A equipe se refere a isso como o "efeito gaiola, "já que a estrutura de encapsulamento se assemelha a uma gaiola.
Se os poros nas gaiolas forem muito grandes, o local ativo é desativado após apenas um ciclo de reação e nunca é reativado novamente. Quando as aberturas dos poros são menores, Contudo, eles coordenam uma dança molecular precisa entre os reagentes e os sítios ativos de ferro - que produz metanol diretamente e regenera o sítio ativo. Aproveitando o chamado 'efeito gaiola, 'a equipe foi capaz de reativar 40% dos sites desativados repetidamente - um avanço conceitual significativo em direção a um processo catalítico em escala industrial.
"O ciclo catalítico - a reativação contínua de locais regenerados - poderia algum dia levar a produção econômica de metanol a partir do gás natural, "disse Snyder, agora um pós-doutorado na UC-Berkeley no Departamento de Química de Jeffrey R. Long.

Benjamin Snyder (à direita) e seu ex-conselheiro PhD, Edward Solomon, professor de química em Stanford e de ciência de fótons no SLAC. Crédito:Linda A. Cicero
Este passo fundamental na ciência básica ajudará a elucidar para os químicos e engenheiros químicos o processo que as zeólitas de ferro usam para produzir metanol em temperatura ambiente, mas ainda resta muito trabalho antes que tal processo possa ser industrializado.
O próximo na lista de Snyder:abordar a realização do processo não apenas à temperatura ambiente, mas usando o ar ambiente em vez de alguma outra fonte de oxigênio, como o óxido nitroso usado nessas experiências. Lidar com um poderoso agente oxidante como o oxigênio, que é notoriamente difícil de controlar em reações químicas, será outro obstáculo considerável ao longo do caminho.
Por enquanto, Snyder ficou satisfeito e surpreso com os poderes ilustrativos da sofisticada instrumentação espectroscópica dos laboratórios Solomon que foram aproveitados para este estudo. Isso foi inestimável para sua compreensão da química e das estruturas químicas envolvidas no processo de metano para metanol.
"É legal como você pode ter uma visão muito poderosa de nível atômico, como o efeito gaiola, a partir dessas ferramentas que não estavam disponíveis para as gerações anteriores de químicos, "Snyder disse.