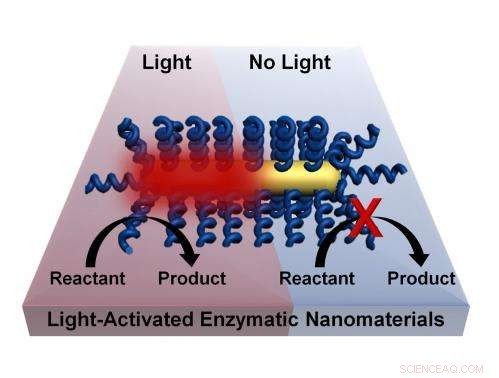
 p Os processos químicos podem ser ativados pela luz sem a necessidade de aquecimento em massa de um material por meio de um processo desenvolvido por pesquisadores da Rice University. A técnica envolve o revestimento de nanobastões com enzimas termofílicas que são ativadas em altas temperaturas. Acender o nanobastão de ouro plasmônico causa um aquecimento altamente localizado e ativa a enzima. Crédito:Lori Pretzer / Rice University
p Os processos químicos podem ser ativados pela luz sem a necessidade de aquecimento em massa de um material por meio de um processo desenvolvido por pesquisadores da Rice University. A técnica envolve o revestimento de nanobastões com enzimas termofílicas que são ativadas em altas temperaturas. Acender o nanobastão de ouro plasmônico causa um aquecimento altamente localizado e ativa a enzima. Crédito:Lori Pretzer / Rice University
p (Phys.org) - a primeira lâmpada desde Edison, o calor tem sido um subproduto indesejável da luz. Agora, pesquisadores da Rice University estão transformando luz em calor no ponto de necessidade, na nanoescala, para acionar reações bioquímicas remotamente sob demanda. p O método criado pelos laboratórios de arroz de Michael Wong, Ramon Gonzalez e Naomi Halas e relatado hoje no jornal American Chemical Society
ACS Nano faz uso de materiais derivados de micróbios únicos - termófilos - que prosperam em altas temperaturas, mas desligam em temperatura ambiente.
p O projeto Rice liderado pelo colega de pós-doutorado Matthew Blankschien e a estudante de graduação Lori Pretzer combina enzimas dessas criaturas com nanopartículas de ouro plasmônico que aquecem quando expostas à luz infravermelha próxima. Isso ativa as enzimas, que são então capazes de realizar suas funções.
p Isso efetivamente permite que processos químicos aconteçam em temperaturas mais baixas. Porque o aquecimento ocorre apenas onde necessário - na superfície da nanopartícula, onde ativa a enzima - o ambiente fica mais fresco.
p Blankschien acha isso fascinante.
p "Basicamente, estamos obtendo os benefícios da fabricação em alta temperatura sem a necessidade de um ambiente de alta temperatura, "disse Blankschien, que ganhou a bolsa de pós-doutorado Peter e Ruth Nicholas há dois anos para trabalhar nessas ideias. “O desafio era manter a temperatura mais alta da nanopartícula, onde a enzima é ativada, de afetar o meio ambiente ao seu redor. "
p A técnica possui grande potencial para processos industriais que agora requerem calor ou se beneficiam do acionamento remoto com luz.
p "As implicações são muito empolgantes, "disse Wong, professor de engenharia química e biomolecular e de química. “Na indústria química, há sempre a necessidade de melhores materiais catalíticos para que possam executar reações de maneira mais econômica, mais 'verde' e mais sustentável. Você não deve usar galões de solvente para fazer um miligrama de produto, mesmo que você consiga vendê-lo por muito dinheiro. "
p Para a indústria, a economia potencial de energia por si só pode fazer com que valha a pena investigar o processo de Rice. "Aqui estamos usando energia 'grátis', "Wong disse." Em vez de precisar de uma grande caldeira para produzir vapor, você liga uma lâmpada de baixo consumo de energia, como um LED. Ou abra uma janela. "
p A partícula no centro do processo é um nanobastão de ouro com cerca de 10 nanômetros de largura e 30 de comprimento que aquece quando atingido por luz infravermelha próxima de um laser. As hastes têm o tamanho e a forma certos para reagir à luz em cerca de 800 nanômetros. A luz excita os plasmons de superfície que ondulam como a água em uma piscina, neste caso, emitindo energia como calor.
p O laboratório Halas 'Rice é famoso por ser o pioneiro no uso de nanoconchas de ouro (um material relacionado) para tratar o câncer, tendo como alvo os tumores com partículas que são aquecidas para matar os tumores de dentro. A terapia está agora em testes em humanos.
p A nova pesquisa assume um rumo um pouco diferente, aquecendo nanopartículas revestidas com um modelo de enzima termofílica, glucoquinase, de Aeropyrum pernix. A. pernix é um micróbio descoberto em 1996 prosperando perto de fontes subaquáticas quentes na costa do Japão. Por volta de 176 graus Fahrenheit, A. pernix degrada a glicose, um processo necessário para quase todos os seres vivos. A enzima pode ser aquecida e resfriada repetidamente.
p Em seus experimentos, Blankschien e Pretzer clonados, enzimas glucoquinase purificadas e alteradas para que se ligassem às nanopartículas de ouro. Os complexos enzima / nanopartícula foram então suspensos em uma solução e testados quanto à degradação da glicose. Quando a solução foi aquecida a granel, eles descobriram que os complexos se tornaram altamente ativos a 176 graus, como esperado.
p Em seguida, os complexos foram encapsulados em uma gota semelhante a um gel de alginato de cálcio, que ajuda a manter o calor, mas é poroso o suficiente para permitir que as enzimas reajam com os materiais ao seu redor. Sob aquecimento em massa, o desempenho das enzimas caiu drasticamente porque os grânulos isolaram as enzimas muito bem.
p Mas quando os complexos encapsulados foram iluminados por contínuos, luz de laser infravermelho próximo, eles funcionaram substancialmente melhor do que sob aquecimento em massa, deixando a solução próxima à temperatura ambiente. Os pesquisadores descobriram que os complexos são robustos o suficiente para semanas de reutilização.
p "Por mais rebuscado que pareça, Acho que as empresas químicas estarão interessadas na ideia de usar luz para fazer produtos químicos, "Wong disse." Eles estão sempre interessados em novas tecnologias que podem ajudar a tornar os produtos químicos mais baratos. "
p Ele vê outros usos possíveis para a nova abordagem na produção de combustíveis a partir da degradação da biomassa como a lignocelulose; para a fabricação de medicamentos sob demanda - talvez de tatuagens infundidas com nanopartículas no corpo; ou mesmo para reduzir as concentrações de açúcar no sangue como uma forma diferente de controlar o diabetes.
p "Que agora podemos fazer essas partículas é ótimo, "Wong disse." A próxima parte emocionante é pensar sobre como podemos implantá-los. "
p Ryan Huschka, um co-autor do artigo, é ex-aluno de pós-graduação da Rice e agora professor assistente de química na Newman University. Halas é o Professor Stanley C. Moore em Engenharia Elétrica e de Computação, um professor de engenharia biomédica, química, física e astronomia e diretor do Laboratório de Nanofotônica de Rice. Gonzales é professor associado de engenharia química e biomolecular e também de bioengenharia
p A pesquisa foi apoiada pelo Programa de Pós-Doutorado Peter e Ruth Nicholas administrado pelo Instituto Richard E. Smalley para Ciência e Tecnologia em Nanoescala, o Programa de Prêmio Hamill de Inovações do Instituto de Biociências e Bioengenharia da Rice University, o Fundo de Iniciativas do Corpo Docente da Universidade Rice, a Fundação Robert A. Welch, a National Security Science and Engineering Faculty Fellowship, a Agência de Redução de Ameaças de Defesa, o Escritório de Pesquisa Científica da Força Aérea e a Fundação Nacional de Ciência.
