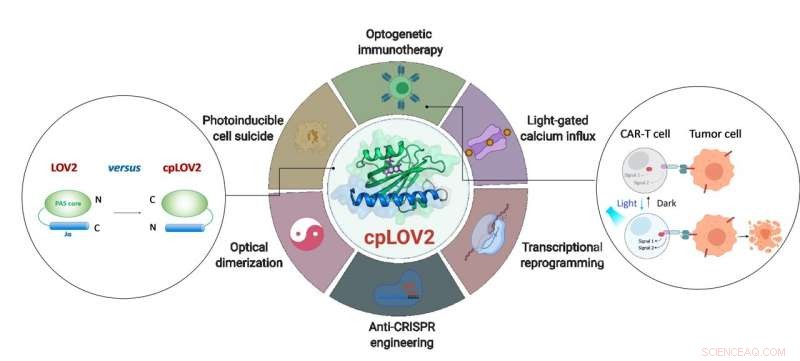
O projeto de cpLOV2 e sua aplicação estendida em engenharia optogenética. Crédito:ZHU Lei
Recentemente, Prof. WANG Junfeng do Laboratório de Alto Campo Magnético dos Institutos de Ciências Físicas de Hefei (HFIPS), junto com estudiosos internacionais, desenvolveu um romance circular de luz-oxigênio-voltagem 2 (LOV2) para expandir o repertório de photoswitches geneticamente codificados, que irá acelerar o design de novos dispositivos optogenéticos. O resultado foi publicado em Nature Chemical Biology .
O domínio LOV2 é um photoswitch sensível à luz azul. Em um dispositivo optogenético baseado em LOV2 típico, um domínio efetor é fundido após a hélice Jα C-terminal de LOV2, com a intenção de enjaular o efetor por meio de impedimento estérico no escuro. Na fotoestimulação, o desdobramento da hélice Jα disparado por luz expõe o domínio efetor para restaurar sua função. A elaboração de uma proteína photoswitchable baseada em LOV2 geralmente exige enormes esforços de engenharia para otimizar cada componente e o linker intermediário. Portanto, é desejável expandir a caixa de ferramentas optogenética atual criando novos módulos que simplifiquem essas etapas.
Neste estudo, os pesquisadores projetaram cpLOV2 usando permutação circular, uma abordagem robusta de engenharia de proteínas, anteriormente usada para desenvolver novas variantes de sondas fluorescentes geneticamente codificadas e biocatalisadores. Os terminais de nitrogênio (N) e carbono (C) de cpLOV2 foram criados no terminal N da hélice Jα, enquanto os antigos foram conectados por um ligante rico em glicina e serina. Portanto, o efetor pode ser fundido antes do Jα N-terminal de cpLOV2 além do C-terminal em LOV2.
Usando espectroscopia de RMN de alta resolução e outras técnicas, os pesquisadores demonstraram que a integridade estrutural e a função da dissociação Jα induzida pela luz de cpLOV2 são bem mantidas. cpLOV2 também foi bem trabalhado em LOVTRAP e dímero induzido por luz melhorado (iLid), ambos são sistemas de heterodimerização óptica baseados em LOV2.
cpLOV2 forneceu mais opções para desenvolvimentos de aplicações optogenéticas. Os pesquisadores geraram uma série de híbridos fundindo LOV2 ou cpLOV2 com diferentes Ca 2+ fragmentos de ativação de canal e de autoinibição derivados da molécula de interação estromal 1, e encontrou vários novos atuadores ópticos baseados em cpLOV2 para o gate ORAI1 Ca 2+ canal, portanto, eles demonstraram que cpLOV2 pode fornecer novas superfícies de encarceramento para superar as limitações associadas ao LOV2 de tipo selvagem.
Para os efetores, é necessário um terminal N livre para executar sua função completa, cpLOV2 é a melhor escolha. Uma proteína chave envolvida na necroptose, proteína semelhante ao domínio de linhagem mista (MLKL), foi o sucesso enjaulado e desencadeado em cpLOV2-MLKL, mas não em MLKL-LOV2, para o controle óptico de suicídios de células.
A terapia com células T de receptor de antígeno quimérico (CAR) surgiu como uma abordagem imunoterapêutica promissora. Contudo, a atividade incontrolável das células T CAR durante a terapia causaria efeitos colaterais graves, e. síndrome de liberação de citocinas em alguns pacientes. Os pesquisadores projetaram sistemas de heterodimerização óptica baseados em cpLOV2 (cpLID), e CAR split foto-ajustável (optoCAR) construído. As células T optoCAR terapêuticas podem ser ativadas especificamente pelo antígeno tumoral CD19 e luz azul, e então proliferar para matar o CD19 + Células de linfoma Raji.
Em modelo de camundongo implantado com CD19 + Células Raji, os pesquisadores usaram nanopartículas de conversão ascendente (UCNPs) para converter a luz infravermelha próxima de alta penetração em tecidos em luz azul e ativar as células T optoCAR injetadas e alcançar uma terapia altamente eficaz de tumor de linfoma. As células T OptoCAR desenvolvidas neste estudo permitem o controle espaço-temporal e reversível das atividades das células T e da produção de citocinas.
Estes resultados encorajadores sugerem que as células T optoCAR podem mitigar os efeitos colaterais potenciais sem perder a eficácia terapêutica. No futuro, eles planejam tentar a imunoterapia optogenética para tratar diferentes tipos de câncer.