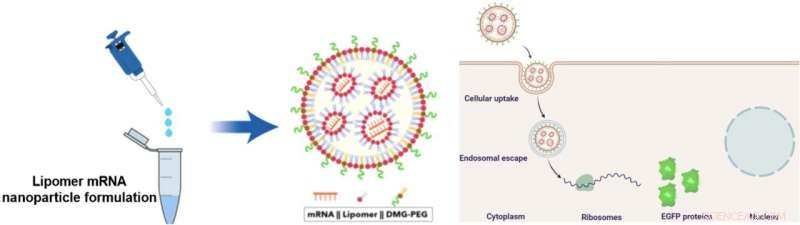
O lipômero é combinado com mRNA e DMG-PEG para formar nanopartículas portadoras de mRNA (NPs). Esses NPs podem contornar o fígado para entregar o mRNA diretamente às células do pulmão. Os cientistas usaram o mRNA que codifica a proteína fluorescente verde aprimorada (EGFP) para a visualização das proteínas. Crédito:Mahmoud M. Abd Elwakil, et al., Horizontes de materiais . 7 de junho, 2021
Os pesquisadores da Universidade de Hokkaido, no Japão, criaram e testaram uma biblioteca de compostos à base de lipídios para encontrar uma maneira de fornecer drogas de RNA aos pulmões com segurança e eficácia. Suas análises, publicado na revista Materials Horizons, localizou um polímero lipídico que pode no futuro ser usado para tratar a síndrome da angústia respiratória aguda, hipertensão pulmonar e câncer de pulmão.
A resposta à pandemia de COVID-19 nos familiarizou com as vacinas de RNA que carregam o código genético nas células para estimular a produção de proteínas virais que ativam nossa imunidade protetora. Os medicamentos de RNA estão mostrando grande potencial para o tratamento de uma grande variedade de outras doenças, direcionando de forma semelhante a produção de proteínas dentro das células, sem a necessidade de inserir ou deletar DNA. Mas os cientistas enfrentam vários desafios em sua entrega segura às células-alvo. Uma abordagem bem-sucedida, mas complexa, envolve transportar os códigos de RNA dentro de nanopartículas cobertas com compostos, chamados ligantes de direcionamento, que podem se ligar a células específicas. Isso funcionou para direcionar as células do fígado.
O cientista farmacêutico Hideyoshi Harashima da Universidade de Hokkaido e o químico de polímeros Toshifumi Satoh lideraram uma equipe de pesquisadores no desenvolvimento e teste de uma biblioteca de compostos à base de ε-decalactona, lipídios que poderiam contornar o fígado - que degrada toxinas e substâncias estranhas - e, especificamente, entregam código de RNA aos pulmões. Harashima recebeu recentemente a Medalha Høst-Madsen, a maior honra científica concedida pela Federação Farmacêutica Internacional (FIP).

O mRNA livre não atingiu nenhum órgão (esquerda), enquanto NPs contendo lipômero AA03-DL-10 transportaram especificamente o mRNA que codifica EGFP para os pulmões e produziram proteínas fluorescentes verdes oito horas após a administração intravenosa em camundongos. Crédito:Mahmoud M. Abd Elwakil, et al., Horizontes de materiais , 7 de junho, 2021
Os cientistas trabalharam com dois compostos em forma de anel intimamente relacionados:ε-caprolactona e ε-decalactona. Nanopartículas lipídicas (NPs) contendo essas lactonas mostraram-se previamente acumuladas nos pulmões. Eles foram submetidos a reações de abertura de anel com um dos onze aminoálcoois. Os produtos resultantes foram posteriormente classificados com base no peso molecular de cada braço. Os produtos foram combinados com mRNA e outro composto denominado DMG-PEG para formar NPs portadores de mRNA. NPs feitos de ε-caprolactona eram instáveis, então a equipe procedeu apenas com os NPs de ε-decalactona.
A equipe testou a entrega de ε-decalactona NPs portadores de RNA primeiro em células cancerosas de laboratório e, em seguida, por via intravenosa em camundongos. Eles usaram o mRNA que codifica a proteína fluorescente verde aprimorada (EGFP) para identificar o destino dos NPs. Em última análise, eles descobriram que a ε-decalactona combinada com um aminoálcool linear chamado AA03 produziu o melhor resultado. As investigações mostraram que os NPs contendo esse lipômero eram capazes de contornar amplamente o fígado e transportar o material de RNA especificamente para os pulmões. Os NPs foram engolfados pela membrana celular e o conteúdo de RNA foi liberado no citoplasma das células pulmonares.
"Mostramos que expandir o espaço químico de materiais inteligentes pode permitir a fabricação de nanopartículas para alvos difíceis de alcançar, sem a necessidade de ligantes de direcionamento, "diz Harashima." Projetar bibliotecas combinatórias que fornecem diversos lipômeros ε-decalactona pode ser uma estratégia fácil e escalonável para o desenvolvimento de terapias genéticas de próxima geração para órgãos além do fígado. "