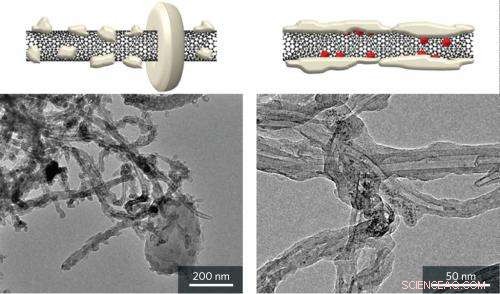
 p Vistas esquemáticas (superior) e imagens de microscopia eletrônica de transmissão (inferior) mostrando cristais rígidos que se formam em nanotubos de carbono descobertos (esquerda) e depósitos amorfos em cátodos de nanotubos de carbono com nanopartículas de óxido de rutênio (RuO2) (direita) após a descarga de lítio-oxigênio (Li –O2) baterias. Crédito:reproduzido, com permissão, da Ref. 1 © 2013 American Chemical Society
p Vistas esquemáticas (superior) e imagens de microscopia eletrônica de transmissão (inferior) mostrando cristais rígidos que se formam em nanotubos de carbono descobertos (esquerda) e depósitos amorfos em cátodos de nanotubos de carbono com nanopartículas de óxido de rutênio (RuO2) (direita) após a descarga de lítio-oxigênio (Li –O2) baterias. Crédito:reproduzido, com permissão, da Ref. 1 © 2013 American Chemical Society
p Lítio-oxigênio não aquoso (Li-O
2 ) as baterias podem armazenar energia em densidades que rivalizam com a gasolina. Comercializando esta tecnologia emergente, Contudo, exigirá avanços que permitirão que as baterias sejam recarregadas com eficiência. Hye Ryung Byon e Eda Yilmaz da Unidade de Pesquisa da Iniciativa RIKEN Byon deram um grande passo em direção a esse objetivo, aumentando significativamente a eficiência de recarga de Li – O
2 baterias através da aplicação criteriosa de óxido de rutênio catalítico (RuO
2 ) nanopartículas. p As baterias Li-O2 eliminam os cátodos de óxido de metal pesado usados em baterias convencionais de íon-lítio para permitir que o lítio reaja diretamente com o oxigênio atmosférico em cátodos feitos de luz, materiais porosos, como nanotubos de carbono. Quando a bateria descarrega, íons de lítio e gás oxigênio reagem para formar peróxido de lítio (Li
2 O
2 ) cristais no cátodo. Para recarregar a bateria, o isolante Li
2 O
2 os cristais devem ser decompostos - uma reação que requer potenciais de recarga significativos, o que pode encurtar a vida útil da bateria.
p Byon e Yilmaz tentaram melhorar a eficiência de recarga da bateria adicionando RuO
2 nanopartículas aos cátodos de nanotubos de carbono. "RuO
2 tem uma energia de superfície ideal para adsorção de oxigênio e é um bom catalisador para reações de oxidação, "explica Yilmaz. No entanto, porque a maioria dos catalisadores à base de rutênio são realizados em soluções aquosas, a equipe teve que agir com cuidado para entender o que aconteceria quando RuO
2 estava cercado por Li sólido
2 O
2 .
p Experimentos revelaram que o novo composto RuO2 / nanotubo de carbono reduziu consideravelmente o potencial de recarga da bateria em comparação com cátodos feitos apenas de nanotubos. Para entender por que, os pesquisadores colaboraram com o Centro de Radiação Síncrotron da Universidade Ritsumeikan em Kyoto para caracterizar os produtos de descarga usando uma série de técnicas, incluindo espectroscopia de absorção de raios-X e microscopia eletrônica. Esses testes revelaram que o Li
2 O
2 depósitos no RuO
2 nanotubos carregados tinham uma morfologia amorfa bastante diferente daquela vista em qualquer outro Li – O
2 sistema de bateria.
p As imagens de microscopia eletrônica mostraram que Li
2 O
2 partículas que se formaram nos cátodos de nanotubos nus tinham grandes, cristais em forma de halo. No RuO
2 / cátodos de nanotubos de carbono, Contudo, uma camada informe de Li
2 O
2 revestiu todo o nanotubo (Fig. 1). A equipe observa que esta camada de Li2O2 tem uma grande área de contato com o cátodo de nanotubo de carbono condutor. Consequentemente, Li
2 O
2 a decomposição pode ser alcançada com menos energia, resultando em maior eficiência da bateria.
p "Este é um dos primeiros estudos que mostram como os catalisadores afetam o Li-O não aquoso
2 baterias; até agora, houve pouco foco no impacto da estrutura de Li2O2 no desempenho da bateria, "diz Byon." Esta pesquisa pode servir como um guia para futuras abordagens alternativas. "
